Как искусственный интеллект трансформирует дизайн лекарств?
Как мы обсуждали ранее, финансирование проектов, связанных с использованием искусственного интеллекта в фармацевтической промышленности в ближайшем будущем будет исчисляться миллиардами долларов, что станет причиной огромного потенциала роста в этом конкретном секторе.
ИИ трансформирует процесс разработки лекарств, делая его более эффективным и действенным, принося пользу всем заинтересованным сторонам — компаниям, разрабатывающим новые лекарства и пациентам, остро нуждающимся в жизнеспособном лечении.

Какова роль применения искусственного интеллекта в обнаружении и разработке лекарств? Эту тему мы продолжаем обсуждать с главным экспертом-биологом и научным аналитиком компании «Semantic Hub» Анной Палеевой.
— Какие команды разработчиков активно используют машинное обучение, чтобы сделать процесс разработки новых лекарственных препаратов более эффективным?
Анна: Среди IT компаний, занимающихся поиском молекул по их структуре — компания Atomwise. Дизайнеры лекарств успешно применили технологию сверточных нейронных сетей, которые обычно используются для технологии распознавания лиц в толпе. Компания адаптировала этот механизм и воспользовалась им для извлечения информации из миллионов экспериментальных измерений аффинности (силы взаимодействия молекул) из тысяч белковых структур, чтобы предсказать связывание малых молекул с белками, для поиска молекулы, которая могла бы быть активной по отношению к вирусу Эболы.
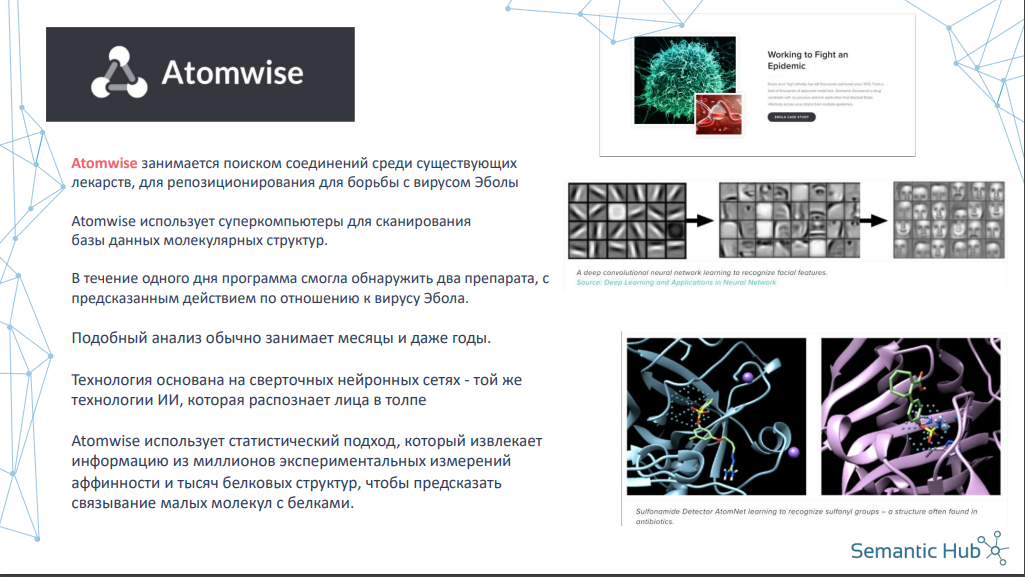 Была проанализирована довольно большая база молекул и найдена подходящая. Это — пример задействования уже существующих технологий для нужд фармкомпании Еще один интересный пример из области доклинических исследований, то есть исследований, проводящихся на клеточных или животных моделях — organ-on-a-chip — это 3D клеточные культуры, в которых можно воспроизвести биологию человека in vitro. На специальное трехмерное микрофлюидное устройство, искусственную мембрану, высаживают клетки лёгких с одной стороны и эндотелиальные клетки с другой, создают давление, кровоток и инфицируют бактериями для моделирования воспалительных процессов, происходящих in vivo в тканях легких.
Была проанализирована довольно большая база молекул и найдена подходящая. Это — пример задействования уже существующих технологий для нужд фармкомпании Еще один интересный пример из области доклинических исследований, то есть исследований, проводящихся на клеточных или животных моделях — organ-on-a-chip — это 3D клеточные культуры, в которых можно воспроизвести биологию человека in vitro. На специальное трехмерное микрофлюидное устройство, искусственную мембрану, высаживают клетки лёгких с одной стороны и эндотелиальные клетки с другой, создают давление, кровоток и инфицируют бактериями для моделирования воспалительных процессов, происходящих in vivo в тканях легких.
Подобные разработки в будущем могут снизить необходимость проведения испытаний на животных.

Третий пример — компания Exscientia, которая разработала первое лекарство, вышедшее на стадию клинических испытаний. Совместно с японской фармацевтической компанией с помощью искусственного интеллекта они разработали препарат DSP-1181, являющийся агонистом 5-HT1A рецептора серотонина. Препарат предназначен для лечения пациентов с обсессивно-компульсивным расстройством (ОКР). Вся разработка заняла один год вместо положенных 5-6 лет, которые обычно уходят у исследователей на этап Drug discovery. В марте этого года должна была стартовать первая фаза клинических испытаний в Японии, но из-за разразившейся пандемии Covid-19 пока нет информации о том, все ли идет по плану.
— В чем заключаются основные цели клинических испытаний? Какое место искусственный интеллект может занимать на стадии клинических испытаний?
Анна: При разработке нового препарата нельзя обойтись без испытаний, проводящихся напрямую на людях, поскольку совершенно невозможна экстраполяции результатов, полученных на животных или на биологических моделях на человека.
Любые клинические испытания могут быть инициированы только после того, как получены уже обнадеживающие результаты в ходе доклинических исследований, а также после их одобрения этическим комитетом и получения положительного решения уполномоченного органа здравоохранения той страны, где планируется проводить исследование.
 Основными целями клинических исследований является оценка эффективности и безопасности нового лекарственного препарата или же расширение показаний к применению уже существующего (repurposing).
Основными целями клинических исследований является оценка эффективности и безопасности нового лекарственного препарата или же расширение показаний к применению уже существующего (repurposing).
В целом, процесс клинических испытаний состоит из нескольких фаз:
- Фаза-ноль — это фаза, на которой происходит оценка фармакокинетики, понимание о биодоступности препарата, периода полувыведения и другие подобные показатели.
- Первая фаза — это тестирование на здоровых добровольцах. Успех этой фазы, примерно, 70 %.
- Вторая фаза — это тестирование на пациентах с целевым заболеванием. Это, как правило, небольшое количество людей от 20 до 200 человек. На данном этапе происходит оценка эффективности и побочных эффектов. Успех второй фазы — около 33 %. Зачастую первую и вторую фазу объединяют в одно большое испытание.
- Третья фаза предполагает тестирование на пациентах, на гораздо большей выборке, от 300 до 3000 человек. Успех этой фазы — 25-30 % .
- Четвертая фаза проводится после выхода препарата на рынок, после одобрения регуляторами. Это наблюдение за долгосрочными последствиями. Четвертую фазу проводят редко, так как она самая дорогая.
Клинические испытания — довольно длительный и очень дорогой этап создания нового препарата, требующий большого числа ручных процессов. Искусственный интеллект уже сейчас помогает улучшению дизайна клинических испытаний, эффективному и быстрому подбору пациентов, оптимизации процессов, анализу результатов клинических испытаний и их сравнению с Real world evidence. RWE – это данные, которые берутся из реальной жизни, от пациентов, которые находятся вне клинических испытаний и обладают спектром коморбидных состояний (сопутствующих заболеваний), прошедших всевозможные терапии. Таким сравнением может заниматься искусственный интеллект, собирая данные Real world evidence, систематизируя их для последующего анализа.

— Какие еще алгоритмы машинного обучения востребованы при разработке новых лекарств?
Анна: Одни компании занимаются автоматизацией анализа гистопатологии, другие — специализируются на подборе пациентов для клинических исследований, оптимизации клинических исследований.
В сфере интересов компании WinterLight Labs — оценка и мониторинг когнитивного здоровья пациентов путем анализа фрагментов речи. В этом случае ИИ применяется для оценки реакции пациентов на терапию для клинических испытаний, связанных с психическим здоровьем.
Еще хочется упомянуть компании, которые создают модели заболеваний и методов лечения, из данных научной литературы и данных Real world evidence от пациентов. Таким образом они имитируют клинические испытания с виртуальными пациентами.
— Какое будущее ждёт искусственный интеллект? Какие проблемы в работе с ним приходится преодолевать сегодня?
Анна: Уже наблюдается некоторая гонка за данными. Фарма нуждается в надежных, проверенных данных, которые будут совместимы между собой, а также максимально конфиденциальны. Любые показания, снятые, например, с носимых устройств пациентов, генетические данные, данные из электронных медицинских карт должны быть максимально конфиденциальными, потому что фармкомпании не имеют права доступа к персональным данным пациентов
Для того, чтобы работать с большими данными, искусственному интеллекту, важна IT инфраструктура, для создания и отладки которой требуется очень много времени, улучшение качества и класса оборудования, специального программного обеспечения, достаточной поддержки, а также обязательное привлечение к разработке медицинских экспертов.
Если разработчики ИИ собираются работать с фармкомпанией, то им нужно будет обязательно сотрудничать с медицинскими R&D департаментом. Или потребуется включить в штат собственных медиков, которые будут помогать в разработке. Пока все вышеперечисленное обходится достаточно дорого.

— Готовят ли институты наших специалистов по ИИ для разработок лекарств?
Анна: Сейчас много сильных институтов, а точнее факультетов. Например, в Высшей Школе Экономики есть факультет компьютерных наук, на котором готовят высококлассных специалистов. Там же есть магистерская программа по анализу данных в биологии и медицине. Так что, да в России можно готовить специалистов для разработки лекарственных препаратов.
— Искусственный интеллект — вопрос развития технологий. Могут ли наши специалисты конкурировать в этой области?
Анна: Да, абсолютно точно, могут. IT в России — до сих пор одна из сильных и развитых отраслей. Много выходцев из нашей страны работают в крупнейших компаниях США — в Google, Microsoft так b других IT-гигантах.

— Какие законодательные проблемы потребуется урегулировать в связи с внедрением ИИ в процесс разработки лекарств?
Анна: На первый план выходит вопрос: кто возьмет ответственность за продукты искусственного интеллекта?
Для этого понадобится пересмотр существующей нормативной базы или даже совершенно новая нормативная база, которая будет устанавливать правильное сотрудничество с регулирующими органами.
Остается открытым вопрос, как, вообще, объяснить принятые искусственным интеллектом решения. Было бы правильно, наверное, использование так называемого объяснимого искусственного интеллекта.
Существует страх перед использованием искусственного интеллекта у медиков, которые могут быть скептически настроены по отношению к подобного рода инновациям. Когда речь идет о здоровье и жизни пациента, понятно, что ошибок быть просто не должно.
Также, есть проблема экстраполяции данных, полученных от искусственного интеллекта на пациентов. Нужны такие системы, которые бы смогли сделать этот перенос реальным.
Остается открытым вопрос этики использования искусственного интеллекта.
— Как сами исследователи относятся к тому, что ИИ играет все более значимую роль на их поле?
Анна: Из-за стремительного развития IT в медицине должна происходить «смена поколений» работников внутри фармы. Сегодняшней сотрудник фармкомпании должен быть гибким, уметь грамотно ориентироваться в цифровом мире, ему необходимо быть открытым и готовым для непрерывного обучения в рамках развития своей карьеры, потому что так быстро и стремительно все меняется, что если ты не успеваешь, то и компания не поспевает за всеми изменениями.

— Какие компании в Российской Федерации занимаются оптимизацией клинических исследований и Real World Evidence (RWE)?
Анна: Системами получения доказательств в условиях рутинной клинической практики в Российской Федерации занимается компания Semantic Hub. Мы анализируем данные, полученные реальных историй пациентов в Интернете (RWE), занимаемся поиском недодиагностированных пациентов с орфанными заболеваниями. Наш подход позволяет улучшить диагностику орфанных заболеваний и доступ пациентов к терапии. Обеспечивает решение следующих задач: выявление пациентов, оценка реакции на терапию, углубленное понимание пути пациента на этапе прелонча (до выхода препарата на рынок), анализ value proposition препарата для задач Market Access и другие.
— Использовался ли искусственный интеллект для быстрой разработки лекарства от коронавируса?
Анна: Я знаю пример разработки очень точной модели коронавируса, и это сделала российская компания Visual Science. Они создали наиболее точную, с точки зрения, структурного анализа, и с точки зрения понимания функций этого вируса модель. Её можно посмотреть на сайте компании, она безумно красивая. Известны несколько разработок препаратов от SARS-CoV-2 с использованием компьютерных технологий. Обзор предварительных результатов разработок лекарств можно прочитать на портале Биомолекула. Я думаю, что большинство компаний, которые сейчас занимаются искусственным интеллектом, для нужд фармацевтических кампаний в той или иной степени ведут такие разработки.
Подготовила Надежда Данилова