10 крупных достижений в сфере медицинских технологий в борьбе с КОВИД-19
На протяжении всей пандемии отрасль медицинского оборудования и диагностики внесла большой вклад в борьбу против КОВИД-19. По данным worldometer.info, в настоящее время в мире зарегистрировано более 64 миллионов случаев заболевания, в результате которых погибло 1,5 миллиона человек.
В этом обзоре мы представим 10 основных достижений в области медицинской техники в борьбе против КОВИД-19.
1. Здравоохранение становится виртуальным и наконец начинает принимать телемедицину

Телемедицина в последние годы медленно и постепенно становилась все более привычной в системе здравоохранения. Пандемия КОВИД-19 ускорила этот процесс на пять лет или около того. По мере того, как вирус подталкивал общество к виртуальному ведению бизнеса, телемедицина становилась естественным решением для пациентов и врачей. Больше не нужно было ждать в поликлиниках, обычные врачебные осмотры стало возможно проводить прямо из квартиры пациента.
Телемедицина действительно вышла на первый план и, по прогнозам, будет иметь сильное присутствие и по завершении пандемии.
2. Быстрый тест на КОВИД-19

Компания Guardant Health уже известна своими тестами для "жидкой биопсии" с целью выявления рака. Тем не менее, эта американская компания произвела фурор в сфере медицинских технологий, когда в августе получила официальное разрешение на экстренное использование своего теста для обнаружения КОВИД-19.
По словам представителей Guardant, тест COVID-19 был тогда использован для того, чтобы помочь университету штата Делавэр безопасно возобновить работу. Испытание также было использовано для поверки здоровья медицинских работников Guardant Health и выбранных партнерских организаций через сертифицированную лабораторию компании.
Согласно заявлению Guardant Health, разработка теста на определение КОВИД-19 была ее "гражданским долгом", и она ни в коем случае не отказывалась от разработки тестов на рак.
3. Совместная работа технологических гигантов

Google и Apple всегда были ожесточенными соперниками, но вирус создал ситуацию, которая потребовала, чтобы они работали вместе. В мае технологические соперники совместно запустили технологию Exposure Notification, которая предназначена для того, чтобы информировать кого-то о возможном заражении, если он вступил в контакт с человеком, которому поставили диагноз КОВИД-19. Такие предупреждения могли получать люди, которые пользовались смартфонами на основе iOS или Android.
В своем совместном релизе "временные партнеры" заявили:
То, что мы создали, не является приложением - скорее это API, который организации общественного здравоохранения смогут включать в свои приложения для установки на телефоны пользователей. Наша технология предназначена для того, чтобы сделать эти приложения лучше. Каждый пользователь может самостоятельно решить, подписываться или нет на сервис Exposure Notification, при этом система не собирает и не использует данных местоположения с устройства. И если человеку поставлен диагноз КОВИД-19, он может сам решать, сообщить об этом в приложении для общественного здравоохранения или нет. Ключом к успеху является адаптация такого сервиса пользователями, и мы считаем, что использованные здесь сильные средства защиты конфиденциальности также являются лучшим способом поощрения использования этих приложений.
4. Устройства для контроля сердечно-сосудистой деятельности стали оказывать влияние на лечение больных КОВИД-19
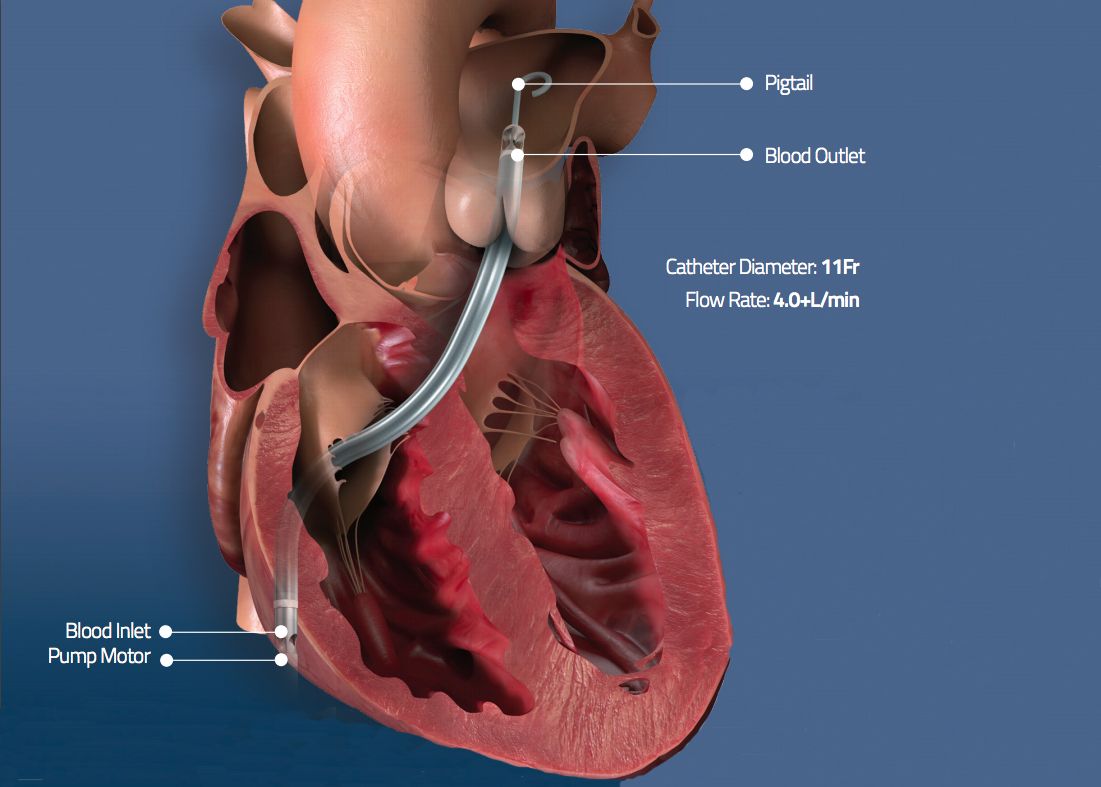
Компания Abiomed была одной из первых организаций на рынке систем контроля сердечно-сосудистого здоровья, которая привлекла внимание и получила разрешение на экстренное использование своей технологии для помощи в лечении симптомов КОВИД-19.
Эта фирма в июне 2020 года получила официальное разрешение на использование своего устройства Impella RP, представляющего собой миниатюрный катетерный сердечный насос для проведения оксигенационной терапии при одновременном снижении нагрузки на сердечные мышцы в случаях, угрожающих жизни, за счет разгрузки сердца и обеспечения механической поддержки кровообращения.
Теперь эта система нашла свое применение в случае COVID-19 у пациентов, страдающих правосторонней сердечной недостаточностью, в том числе с тромбами, блокирующими приток крови в легкие.
Сердечная помпа Impella помогает сердцу перекачивать кровь к аорте – главной артерии, несущую обогащенную кислородом кровь от сердца к телу, и предназначена для поддержки пациентов с COVID-19, которые проходят терапию с использованием экстракорпоральной мембранной оксигенации и у которых развивается отек легких или миокардит.
Как заявил доктор медицины Шон Чакрабарти (Shon Chakrabarti) из медицинского отдела компании Abiomed,
Мы определенно видим сосудистый эффект у больных КОВИД-19. Мы наблюдаем, что это заболевание вызывает протромботическую среду у некоторых пациентов. У некоторых из них острая легочная эмболия и наше устройство потенциально может спасти множество жизней.
Разрешение на применение аппарата Abiomed было тем более значимым, потому что оно пролило свет на потенциальный ущерб, который может нанести сердцу КОВИД-19.
5. Резкий рост финансирования цифрового здравоохранения

Привлечение венчурного капитала в начале глобальной пандемии было значительной проблемой для многих производителей медицинских устройств. Но для компаний, занимающихся цифровым здравоохранением, ситуация выглядела совсем иной. В июне американская аналитическая компания Mercom Capital Group сообщила, что объем инвестиций в цифровое здравоохранение в первой половине 2020 г. был на 24% больше, чем в первой половине 2019 г., когда на рынок пришли 5,1 млрд долл. И это несмотря на то, что пандемия нанесла тяжелый удар мировой экономике.
Резкий скачок финансирования был вызван более широким внедрением цифровых технологий и продуктов во время вспышки КОВИД-19, отметили специалисты Mercom.
Наиболее финансируемыми категориями цифрового здравоохранения в первом полугодии 2020 г. были следующие:
- телемедицина - $1,9 млрд;
- аналитика - $826 млн;
- mHealth-приложения - $794 млн;
- системы поддержки клинических решений - $545 млн;
- системы резервирования приема у врача - $325 млн;
- носимые устройства - $321 млн.
6. Medtronic выкладывает в открытый доступ конструкторскую документацию своего аппарата для искусственной вентиляции легких
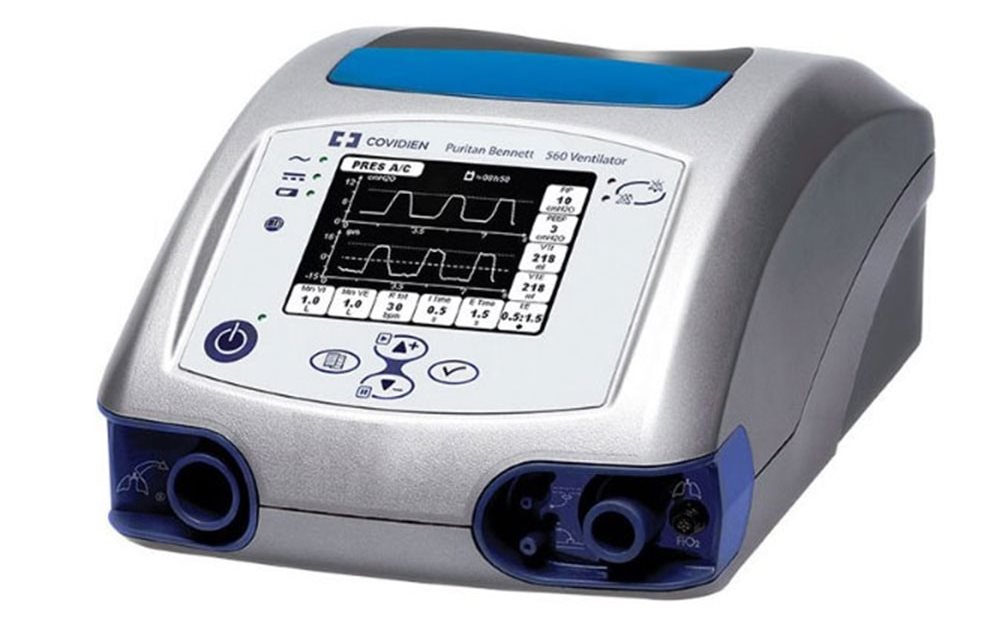
В начале пандемии усилилась озабоченность в связи с нехваткой аппаратов искусственной вентиляции легких на рынке здравоохранения. Это привело к тому, что даже многие фирмы из автомобильной промышленности начали разработку и производство таких дыхательных аппаратов. Этим занялась даже компания-производитель браслетов для фитнеса Fitbit, которая получила разрешение на экстренное использование своего вентилятора.
Компания Medtronic также отозвалась на этот вызов и публично поделилась конструкторскими спецификациями на одну из моделей своего аппарата для искусственной вентиляции легких - Puritan Bennett 560 (PB 560). Этот шаг позволил компаниям, работающим в разных отраслях промышленности, оценить варианты для быстрого производства вентиляторов, чтобы удовлетворить острую потребность в большем количестве таких устройств для пациентов с КОВИД-19.
7. Пятиминутный тест от Abbott

Abbott Laboratories уже неоднократно вызывала интерес профессиональной прессы благодаря своим тестам COVID-19. Тем не менее, тестовые наборы компании стали главной темой обсуждения, когда была представлена BinaxNOW COVID-19 Ag Card - тест на антиген КОВИД-19, позволяющий получить результат через 5-15 минут. Компания получила официальное разрешение на использование этого теста в августе 2020 года.
Благодаря доступной цене и гарантированному быстрому результату тест был признан меняющим правила игры в этой сфере.
8. Управление по контролю за качеством пищевых продуктов и медикаментов (FDA) теперь не регулирует применение лабораторных тестов
Август стал в США поворотным моментом в регулировании тестов на КОВИД-19 и лабораторных тестов в целом.
Министерство здравоохранения и социальных служб США сообщило, что, по его мнению, Управление по контролю за качеством пищевых продуктов и медикаментов (U.S. Food and Drug Administration, FDA) не должно будет требовать предварительного согласования разработанных лабораториями тестов в виду отсутствие четких правил, необходимых для получения разрешения этого государственного ведомства.
Далее в сообщении говорится, что "лица, запрашивающие одобрение или разрешение на чрезвычайное использование тестов, могут, тем не менее, добровольно представить заявку на предварительное одобрение, но не обязаны этого делать, и FDA вынесет решение по этим заявкам".
Согласно материалу, опубликованному в The Washington Post, такая политика министерства стала шоком для FDA.
9. Стандартизация тестов на антитела

На рынке творилась неразбериха с тестами на антитела. Они разные у разных производителей тестов и в настоящее время не могут быть проанализированы и сравнены, так как нацелены на различные белки вируса SARS-CoV-2. Для решения этой проблемы компания Siemens Healthineers объединилась с Центрами по контролю и профилактике заболеваний США, а также с Объединенным исследовательским центром Европейской комиссии для стандартизации тестов.
В рамках этого проекта немецкая компания разрабатывает процесс стандартизации анализов SARS-CoV-2 путем привязки каждого белка к титру нейтрализующего антитела - уровню присутствующего антитела, блокирующему проникновение вируса в клетки в ходе лабораторных экспериментов. Пороговые значения, отображаемые в стандартизированной единице измерения для антител IgG, которые появляются либо от естественной инфекции, либо от вакцинации, могут, вероятно, способствовать стандартизированной интерпретации иммунитета через результаты тестов.
10. Американский регулятор изменил свою стратегию своих действий
В конце января 2020 года Управление по контролю за продуктами и лекарствами США (FDA) разработало стратегию борьбы с КОВИД-19, которую мы наблюдаем в действии сегодня в США и некоторых других странах. Частью этой стратегии было использование метода авторизации применения медицинских решений в условиях чрезвычайной ситуации (Emergency Use Authorization), возникшей из-за пандемии. FDA заявила, что будет работать с межведомственными партнерами-разработчиками продуктов, международными партнерами и глобальными регуляторами, чтобы ускорить разработку и доступность медицинских продуктов, необходимых для диагностики, лечения, смягчения и предотвращения вспышек эпидемии.
Когда FDA представила свою стратегию было зарегистрировано всего немногим более 4000 случаев заражений вирусом, которые были подтверждены в Китае. Более 100 человек стали жертвами этого заболевания - однако, в то время в США не погиб еще ни один человек. Такая быстрая реакция государственного ведомства стала примером организации действий для многих стран.
По материалам MedTech Innovations, MDDI Online, MobiHealth News.