Руки-ножницы: технологиям CRISPR прочат бурное развитие
Журнал Science включил в десятку лучших научных прорывов 2021 года использование технологии CRISPR in vivo. Издание назвало достижением, то, что внедрение CRISPR-Cas9 непосредственно в организм человека позволило снизить содержание токсичного белка в печени и улучшить зрение у двух пациентов с наследственной слепотой.
Состояние мирового рынка
Прошло всего два года с тех пор, как Дженнифер Дудна и Эммануэль Шарпантье получили Нобелевскую премию по химии за работу над технологией CRISPR, а она уже стала инструментом, который ученые и врачи широко используют для изучения средств борьбы с раком, инфекциями, аллергиями и редкими заболеваниями. Согласно отчету Quince Market Insights, по итогам 2021 года рынок CRISPR достиг 900,21 млн долларов. В следующие несколько лет он будет расти с рекордным среднегодовым темпом в 23,8%.
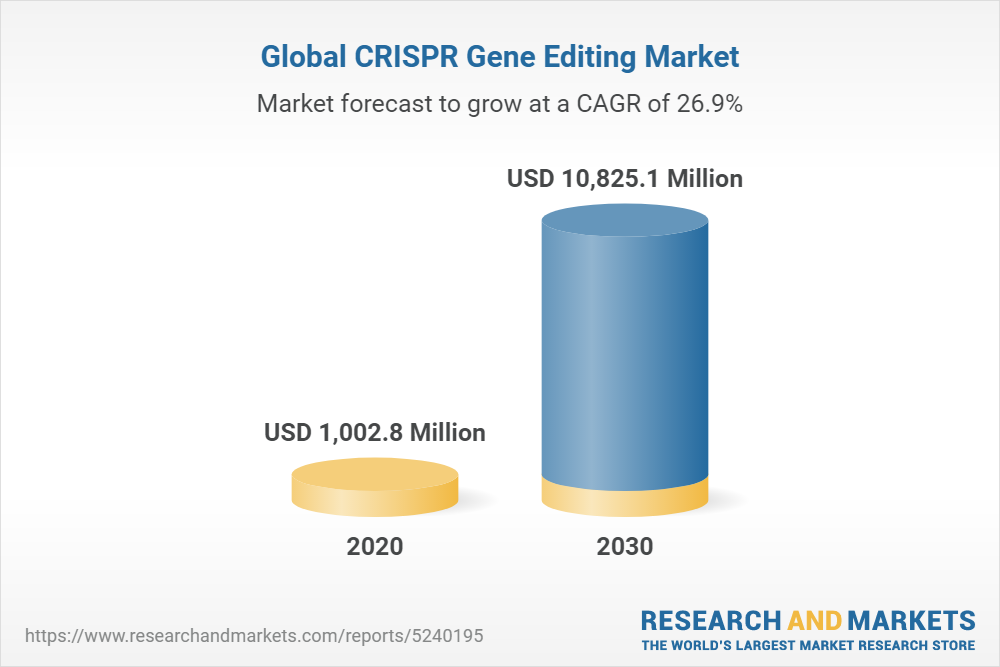
По оценке ReportLinker, глобальный рынок редактирования генов CRISPR достигнет 18,8 млрд долларов к 2031 году. Прогноз аналитиков этого агентства тоже оптимистичен: среднегодовой темп роста в течение предстоящих девяти лет составит 29,6%.
В зависимости от сферы применения рынок технологий CRISPR делится на биомедицину, сельское хозяйство и промышленность. Ожидается, что биомедицинский сегмент будет самым быстрорастущим в течение следующих шести лет.
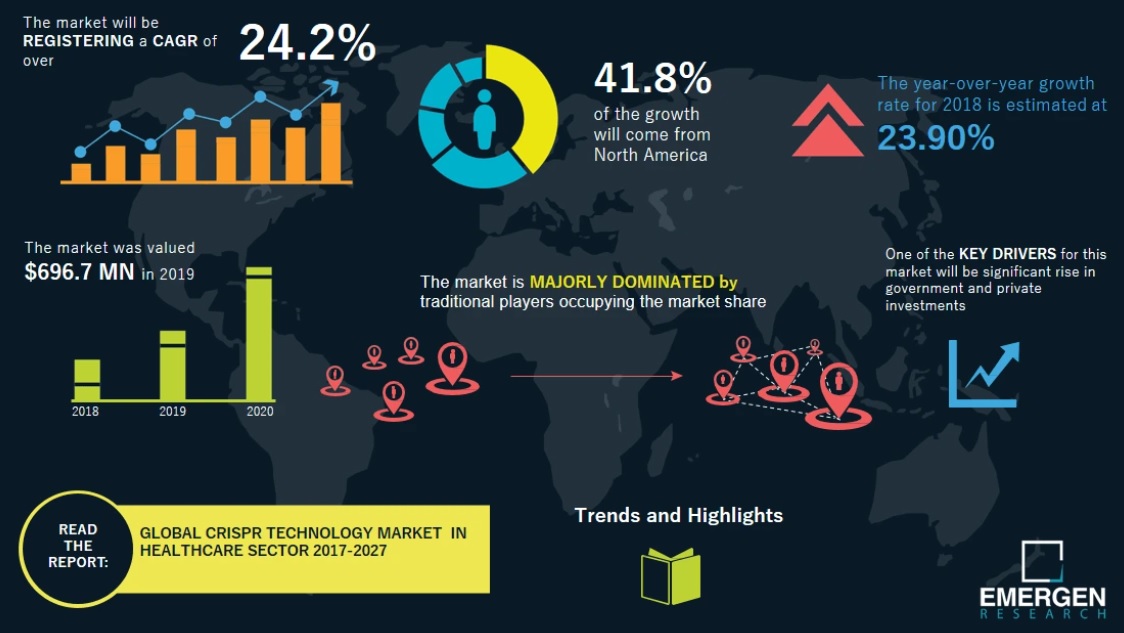
Повышенное внимание к здравоохранению привело к увеличению государственного и частного финансирования исследований в области CRISPR.
Рост числа генетических нарушений также способствует увеличению рыночного спроса на “генетические ножницы”, констатируют аналитики Research & Markets. По данным Национального центра биотехнологической информации США, хотя генетические заболевания встречаются редко, они составляют около 80% редких заболеваний, число которых исчисляется тысячами. Огромное количество необычных болезней подразумевает, что ими страдает один из каждых 17 человек.
Стоимость секвенирования будет снижаться из-за бурного развития технологий.
Набор инструментов для редактирования также продолжает расширяться за счет создания молекул, способных точно вырезать большие фрагменты ДНК, и новых инновационных методов доставки механизмов, изменяющих гены, в клетки. CRISPR становится общим термином для целого комплекса молекулярных систем, которые ученые используют для перезаписи исходного биологического кода окружающего нас мира.
Согласно прогнозу Grand View Research, Inc., рынок реагентов для секвенирования достигнет 21,1 млрд долларов к 2022 году. Существует несколько основных целевых рынков реагентов для секвенирования. Первый рынок — это крупномасштабное производство молекул ДНК и РНК, которые затем используются для создания специализированных продуктов, таких как вакцины. Второй — предназначен для исследований болезней человека, где реагенты позволяют ученым изучать, как работают определенные гены или какие белки действуют в организме. Третий рынок — это судебная экспертиза, где реагенты используются для выяснения того, кто что-то сделал и когда. Четвертый — ориентирован на людей с редкими заболеваниями, которые хотят знать, есть ли у них мутации в генетическом коде.
Северная Америка лидирует
Наибольшую долю на рынке технологий CRISPR занимает Северная Америка. Однако ожидается, что в ближайшие шесть лет Азиатско-Тихоокеанский регион станет самым быстрорастущим регионом.
В 2015 году в США была образована компания Locus Biosciences, которая сегодня является ведущим мировым разработчик продуктов на основе систем CRISPR-Cas3. В 2019 году она объявила о соглашении с Janssen Pharmaceuticals, Inc., направленного на разработку уникальных продуктов на основе рекомбинантного сконструированного CRISPR-Cas3 бактериофага crPhage для лечения серьезных инфекций дыхательных путей.
В то время как другие используют CRISPR-Cas9 для редактирования ДНК в клетках человека и других организмах, Locus концентрирует свои усилия на удалении смертельных патогенов из человеческого организма. CRISPR-Cas3, загруженный в средство доставки бактериофагов, является идеальной системой для нацеливания на ДНК, чтобы разрушить геном бактериальной клетки без возможности восстановления.
Проще говоря, Cas3 действует как Pacman, который поглощает десятки тысяч пар оснований ДНК, в то время как Cas9 действует как ножницы, которые делают точный разрез в нужном месте.
Недавно компания завершила первое в мире плацебо-контролируемое клиническое исследование фазы 1b продукта бактериофага, предназначенного для лечения инфекции мочевыводящих путей, вызванной кишечной палочкой. Ожидается, что к 2023 году в клиническую программу Locus Biosciences войдут еще пять программ по инфекциям мочевыводящих путей, дыхательных путей и кровотока.
В Пенсильванском университете в Филадельфии врачи и исследователи использовали CRISPR для генной инженерии иммунных клеток, чтобы лучше бороться с опухолями.
Эдвард Штадтмауэр, доктор медицинских наук, руководитель отдела гематологических злокачественных новообразований в Медицинской школе Перельмана Пенсильванского университета и главный исследователь клинических испытаний, начал работать над этим проектом в 2016 году, когда технология CRISPR была еще совсем новой. В конечном счете его команда смогли взять Т-клетки пациента, удалить три гена и добавить один ген, что продлило жизнь иммунной клетки и сделало ее более эффективной в борьбе с раком. Это было первое исследовательское использование множественных правок с CRISPR для изменения генома человека.
В 2017 году в сотрудничестве с Техническим общественным колледжем Делавэра компания Rockland создала CRISPR in a Box™, образовательный комплект, который дает учащимся старших классов и муниципальных колледжей инструменты для изучения и использования CRISPR в классе. Вместе с продуктом потребитель получал доступ к учебным видеороликам и возможность пообщаться с учеными через Zoom.

В 2019 году в США был создан стартап Capsida Biotherapys, который использует генную терапию для лечения тяжелых заболеваний. В июне 2021 года фирма объявила о сотрудничестве с CRISPR Therapeutics, пионером в области генной медицины, для совместной разработки методов лечения двух необычных заболеваний: болезни Лу Герига или бокового амиотрофического склероза (БАС) и атаксии Фридрейха.
В марте 2021 года ученые из Калифорнийского университета в Лос-Анджелесе и Калифорнийского университета в Сан-Франциско, Калифорнийского университета в Беркли получили разрешение Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) на совместный запуск ранней фазы первого клинического испытания генной коррекции CRISPR на людях. Речь идет о лечении пациентов с серповидно-клеточной анемией (наследственное заболевание крови, которое может вызывать сильную боль, повреждение органов и преждевременную смерть) с использованием собственных кроветворных стволовых клеток больного.
Хотя клинические испытания еще находятся на ранних стадиях и в них приняли участие всего несколько пациентов, первые результаты ученые называют многообещающими.
Серповидноклеточная анемия, от которой страдают около 100 тыс. человек, живущих в Соединенных Штатах, и миллионы людей во всем мире, является результатом генетической мутации, которая приводит к образованию аномального типа гемоглобина, белка, который эритроциты используют для доставки кислорода по всему телу. Аномальные клетки приобретают серповидную форму и могут сгущаться в узких кровеносных сосудах. На данный момент трансплантация костного мозга от здорового донора является единственным методом лечения, но этот метод может иметь серьезные осложнения.
В сентябре 2021 года еще одна американская компания Editas Medicine объявила о положительных начальных клинических данных продолжающегося открытого клинического исследования фазы 1/2 BRILLIANCE EDIT-101. EDIT-101 находится в стадии разработки для лечения слепоты из-за врожденного амавроза Лебера 10 (LCA10), дегенеративного заболевания сетчатки , связанного с CEP290 .
Ученые рассказали, что положительный профиль безопасности наблюдался в течение 15 месяцев, в основном с легкими побочными эффектами, связанными с самой процедурой инъекции сетчатки. Они будут продолжать увеличивать дозы лечения, чтобы следить за улучшением результатов, и намерены сделать это лечение доступным для детей.
Чей CRISPR?
По данным журнала Built with Biology, все больше стран подают заявки на патенты CRISPR — со скоростью 200 штук в месяц. При этом на сегодня день ни одна организация не получила лицензии на все права интеллектуальной собственности CRISPR-Cas9.
Авторы статьи “Осмысление битвы за патентные права CRISPR-Cas9” в журнале Osler полагают, что “хотя это, вероятно, окажет минимальное влияние на фундаментальные исследования с использованием данных инструментов (из-за особенностей законодательства), любым терапевтическим или коммерческим проектам придется подождать до тех пор, пока юридические разногласия не будут разрешены”.
Как бы то ни было, эксперты единодушны: в 2022 году продолжится стремительное развитие технологий генной терапии и редактирования генов, что приведет к появлению новых компаний и инвестиций в отрасли. По мере продвижения этих технологий в клиниках в ближайшие годы мы увидим их более широкое применение для лечения генетических заболеваний.
Что касается России, то по итогам Совета по науке и образованию 2018 года, президент Владимир Путин “поставил задачу в кратчайшие сроки разработать программу геномных исследований”. В 2019 году она была утверждена.
Программа рассчитана до 2027 года. Как указано в пояснительной записке на сайте Правительства РФ, документом предусмотрены создание и развитие на базе научных и образовательных организаций лабораторий и центров, проводящих исследования в области генетических технологий, их техническая поддержка, проведение научных исследований и разработок с применением генетических технологий, включая разработку биологических препаратов, диагностических систем и иммунобиологических средств для здравоохранения.
В рамках реализации программы предполагается разработка с помощью генетических технологий in vitro и in vivo моделей заболеваний человека, создание биоинформационных и генетических баз данных, создание трех центров геномных исследований мирового уровня. В соответствии с распоряжением Правительства от 26 октября 2019 года, этим центрам в 2019-2024 годах предусмотрены гранты в форме субсидий из федерального бюджета на общую сумму более 11 млрд руб.

Однако практики отмечают, что система логистики, доставки реактивов и оборудования у нас в стране пока оставляет желать лучшего. К тому же катастрофически не хватает генетиков, иммунологов, биоинформатиков, а без них сделать что-либо прорывное и фундаментальное практически нереально.
Текущее состояние науки, а также этические проблемы, связанные с использованием CRISPR, разработку нормативно-правовых актов будут обсуждать 7-9 марта этого года, в Лондоне, на Третьем международном саммите по редактированию генома человека.
Корреспондент МВ и ФВ Екатерина Погонцева специально для evercare.ru