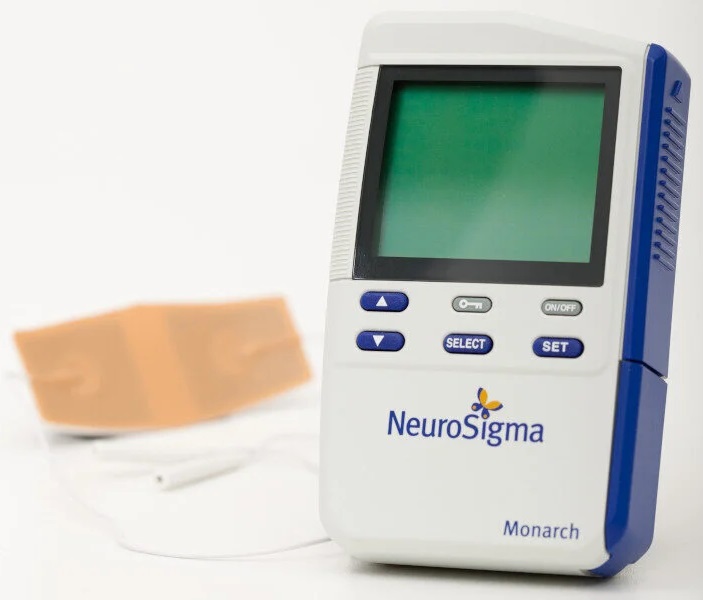
NeuroSigma разработала носимое устройство для лечения СДВГ
Компания NeuroSigma получила одобрение американского регулятора отрасли здравоохранения — Управления по контролю за продуктами и лекарствами США (FDA) — на применение системы внешней стимуляции тройничного нерва (eTNS) Monarch второго поколения для лечения детского синдрома дефицита внимания и гиперактивности (СДВГ).
Monarch eTNS 2.0 работает за счет подачи слабых электрических импульсов на тройничный нерв — главный черепной нерв, участвующий в различных сенсорных функциях.
Устройство предназначено для альтернативного лечения детей в возрасте от семи до 12 лет, которые не используют рецептурные препараты для лечения СДВГ.
Сейчас компания NeuroSigma завершает набор испытуемых для участия в двух двойных слепых многоцентровых испытаниях в США и Великобритании, которые пройдут во втором квартале текущего года. В ходе других испытаний, которые начались в ноябре 2022 года, изучается технология eTNS в педиатрических и подростковых группах с СДВГ.
В испытании 1 фазы ADHD-GEMS примут участие 225 детей из больницы Калифорнийского университета и детской больницы Сиэтла, которые пройдут четырехнедельную двойную слепую фазу исследования с последующим наблюдением в течение одного года. В исследовании 2 фазы, получившем название ATTENS, примут участие до 150 детей и подростков в медицинских центрах Королевского колледжа Лондона и Саутгемптонского университета. В ходе исследования будет проведен сбор данных функциональной магнитно-резонансной томографии у 50 пациентов для изучения механизма действия eTNS.
Директор NeuroSigma Томас Пасхалл сказал:
Monarch 2.0 — это масштабируемая аппаратная платформа, которая будет способствовать быстрой коммерциализации не только в США, но и в Китае, Сингапуре, Корее и, в конечном итоге, по всему миру. Компания NeuroSigma продолжит создавать базу данных мирового класса для СДВГ и других показаний, таких как лекарственно-устойчивая эпилепсия и расстройства аутистического спектра.