FDA выдало разрешение на использование аппарата для "дыхательного диализа" компании ALung
Американский регулятор отрасли здравоохранения (FDA) выдал разрешение на использование для нового типа устройства жизнеобеспечения от компании ALung Technologies, которое помогает удалять углекислый газ из кровотока перед возвращением его в организм, подобно аппарату для диализа.
Это первое такое разрешение для устройства, предназначенного для тяжелобольных пациентов с острой, но обратимой дыхательной недостаточностью. В нем используется метод, известный как низкопоточное экстракорпоральное удаление углекислого газа или ECCO2R.
Система Hemolung в начале прошлого года получила от FDA экстренное разрешение на использование для пациентов с легочной недостаточностью, вызванной COVID-19. Полное разрешение регулятора открывает возможность использования оборудования не только для пациентов с COVID, но и для всех взрослых людей на срок до пяти дней в случаях, когда традиционные аппараты искусственной вентиляции легких не могут адекватно контролировать уровень углекислого газа и рН крови.
Это универсальное устройство подключается к центральной вене пациента с помощью одного катетера и медленно обменивает кровь со скоростью от 350 до 550 миллилитров в минуту.
Система также была сертифицирована в Европе в 2013 году.
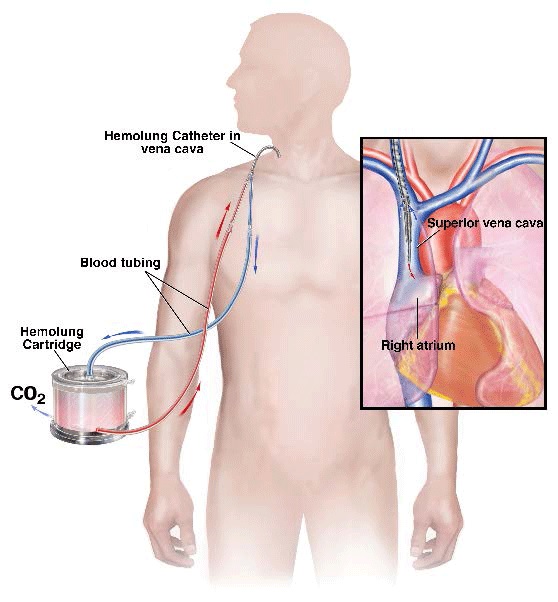
"Hemolung станет новым важным методом лечения острой дыхательной недостаточности, позволяющим избежать или уменьшить вред от инвазивной механической вентиляции", - сказал в своем заявлении медицинский директор компании ALung Стивен Конрад.
У пациентов с дыхательной недостаточностью часто наблюдается повышение уровня углекислого газа, даже если они получают достаточно кислорода. Это заставило многие отделения интенсивной терапии из-за отсутствия доступных альтернатив прибегнуть к использованию более сложного высокопоточного оборудования, которое берет на себя всю работу, выполняемую легкими - аппаратов экстракорпоральной мембранной оксигенации, или аппаратов ECMO.
Как заявил генеральный директор компании ALung Питер ДеКомо,
Для того чтобы продемонстрировать преимущества новой технологии, компания ALung представила в FDA данные о клинической безопасности более 1000 процедур с использованием Hemolung и данные об эффективности, основанные на использовании устройства в более, чем 230 процедурах. Эта информация вместе со всеми нашими доклиническими данными продемонстрировали FDA преимущества Hemolung для терапии ECCO2R.
В настоящее время компания ALung также проводит отдельное клиническое исследование с участием людей с хронической обструктивной болезнью легких (ХОБЛ), чтобы выяснить, может ли система Hemolung помочь пациентам с обострениями ХОБЛ избежать необходимости инвазивной вентиляции.
По словам компании, на данный момент в рандомизированном исследовании приняли участие более 110 человек, а всего планируется набрать около 180 пациентов. Кроме того, по меньшей мере 120 пациентов с тяжелой дыхательной недостаточностью COVID-19 уже прошли курс лечения с помощью Hemolung.