Технологии продолжительного мониторинга артериального давления: перспективы практического применения
Г.С. Лебедев, И.А. Шадеркин, Э.Э. Порубаева, А.И. Шадеркина
Первый Московский государственный медицинский университет им. И.М. Сеченова (Сеченовский университет)
ВВЕДЕНИЕ
Артериальная гипертензия (АГ) является наиболее распространенным хроническим заболеванием, а также единственным важнейшим фактором риска уменьшения продолжительности жизни и снижения ее качества [1]. По данным зарубежных исследований, распространенность АГ составляет 30-45% среди взрослого населения, по данным российских исследований – около 40%. По оценкам экспертов, к 2025 году число лиц с АГ в мире увеличится на 15- 20%, достигнув 1,5 млрд человек, что составляет пятую часть от всего населения Земли [2]. Опасность АГ заключается в развитии таких состояний, как инсульт или инфаркт миокарда, возникающих внезапно и являющихся жизнеугрожающими состояниями. В то же время необходимо отметить, что АГ является контролируемой и устранимой проблемой, так как возникновение данных осложнений возможно спрогнозировать и предотвратить при условии достижения и контроля целевых показателей артериального давления (АД). Это становится возможным благодаря непрерывному/продолжительному измерению АД и своевременному приему лекарственных препаратов в соответствии с его результатами. В виду этого, невозможность справиться с ростом заболеваемости АГ отчасти обусловлена несовершенством инструментов для непрерывного мониторинга АД. Сахарный диабет, который также является одной из серьезнейших угроз для здоровья населения общемирового масштаба, на данном этапе возможно контролировать с помощью специальных носимых устройств, которые осуществляют мониторинг уровня глюкозы в крови и автоматическое поступление инсулина в организм по мере необходимости [3,4]. Это позволяет не только снизить риск развития серьезных осложнений, но и повысить качество жизни пациента в целом, поскольку мониторинг осуществляется автоматически. Аналогичное решение для контроля уровня АД позволило бы значительно снизить возникновение осложнений, представляющих угрозу для жизни. Компактные носимые устройства позволят непрерывно регистрировать важнейшие параметры сердечно-сосудистой системы и тем самым сделают возможным разработку индивидуального подхода к диагностике и терапии сердечных, сосудистых и легочных заболеваний. В данной работе рассмотрены методы неинвазивного измерения АД, предназначенные для его непрерывного и длительного мониторирования.
МАТЕРИАЛЫ И МЕТОДЫ
В ходе работы выполнен анализ данных научной литературы из базы данных Medline, были сформированы поисковые запросы с использованием Mesh «Blood pressure monitors [Mesh]», получено 476 результатов, «Blood pressure monitoring, Ambulatory [Mesh]» – 2647 результатов, а также поисковые запросы «Cuffless blood pressure monitoring», получено 63 результата, «blood pressure monitoring» – 46116, «pulse wave and blood pressure» – 10510, «pulse wave and arterial hypertension» – 4656, «implantable blood pressure» – 1234, «arterial pressure» – 148062, «tattoo blood pressure» – 11 результатов. Глубина основного поиска составляет 10 лет, однако некоторые фундаментальные источники датируются более ранними годами.
РЕЗУЛЬТАТЫ
По мере развития технологий в медицине появляется все больше инноваций и в сфере измерения АД. На данном этапе существует достаточно большое количество устройств для его определения, однако «золотым стандартом» среди неинвазивных методов продолжает оставаться измерение АД по тонам Короткова [5]. С показателями АД, полученными при помощи этого метода, принято сравнивать данные, получаемые с новых приборов. Несмотря на появление новых технологий внимание исследователей направлено также и на усовершенствование данного метода. Так например, Wu H. и соавт. для более точного выслушивания тонов Короткова при измерении манжетным тонометром предложили использование набора Accutension, состоящего из микрофона и мобильного приложения для смартфона [6]. В данном случае микрофон, расположенный под манжетой, регистрирует тоны Короткова, которые затем поступают на подключенный смартфон. Данный прибор может работать как самостоятельно, так и совместно с обычными тонометрами. Исследование точности прибора было проведено на 32 пациентах в возрасте от 24 до 83 лет. У 92,68% показателей систолического АД и 96,34% диастолического АД разница между Accutension и ртутным сфигмоманометром составила <5 мм рт. ст., что соответствует критериям Американской ассоциации содействия развития медицинской техники (American Association for the Advancement of Medical Instrumentation, AAMI).
Peng R.C. и соавт. предложили использовать микрофон смартфона для регистрации сердечных звуков [7]. Данные звуки связаны с сокращениями и расслаблениями предсердий, движениями клапанов, а также током крови, проходящим через сердце [8]. Сигналы, получаемые с помощью микрофона, проходят ряд преобразований для получения значений АД (рис. 1). Исследование прибора было проведено на 32 участниках, и данный метод вычисления АД показал более высокие результаты по сравнению с методами вычисления с помощью времени распространения пульсовой волны (pulse transit time, PTT). Результаты исследования были статистическими значимыми (p<0,05). Точность полученных значений АД соответствовала требованиям AAMI.
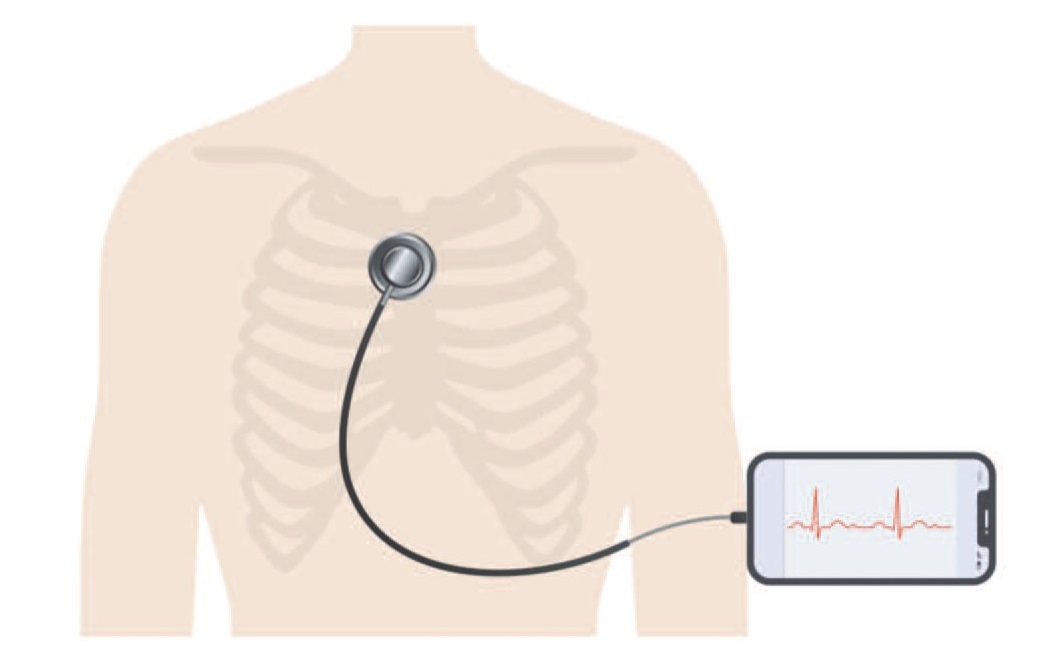
Рис. 1. Схематический рисунок внешнего вида устройства: стетоскоп передает сердечные звуки на телефон с помощью подключения к микрофону телефона
Fig.1. Schematic diagram of device: stethoscope sends heart sounds to the smartphone using its microphone
На данном этапе наиболее распространен осциллометрический способ измерения АД, при котором электронный тонометр автоматически фиксирует колебания воздуха в манжете при пульсации артерии [9]. Необходимо отметить, что данная технология находит применение в форме носимых устройств. В частности, устройство Omron HeartGuide (рис. 2) предназначено для измерения АД на запястье и отличается от большинства конкурентных приборов тем, что оно уже имеет разрешение на продажи и использование от Управления по контролю за продуктами и лекарствами США (Food and Drug Administration, FDA) [10].

Рис. 2. Устройство Omron HeartGuide
Fig. 2. Omron HeartGuide
Другим манжетным прибором, в основе работы которого лежит классический осциллометрический метод, является браслет H2-BP (рис. 3) [11]. Преимуществом данного браслета является измерение АД только на лучевой артерии. Это позволяет избежать проблем, связанных с привычным манжетным измерением, при котором происходит сдавление как лучевой, так и локтевой артерий, что приводит к дискомфорту у пациента и является препятствием для постоянного мониторинга. В 2017 году устройство получило одобрение Корейского Управления по контролю качества продуктов лекарств (Korean Food and Drug Administration, KFDA) на регистрацию в качестве медицинского прибора.

Рис. 3. Устройство H2-BP
Fig. 3. H2-BP
Несмотря на все недостатки манжетного мониторинга АД, существуют решения, использующие манжету, однако избегающие основных проблем, связанных с этим видом измерения. Например, прибор Finometer представляет собой манжету, надеваемую на палец и позволяющую сохранять постоянный диаметр исследуемой артерии [12]. В данном случае для уменьшения гидростатической разницы в давлении палец с манжетой должен находиться на уровне сердца. Кроме того, данный прибор содержит датчик фотоплетизмографии (см. далее), позволяющий определять объем крови в сосуде. Измерения АД проводились на 46 участниках при помощи анероидного сфигмоманометра, исследуемого прибора Finometer и амбулаторного монитора для измерения АД (A&D Australasia Pty Ltd, Thebarton, South Australia, Australia). Показания систолического и диастолического давления амбулаторного прибора были выше, чем у аускульторного и Finometer. Между анероидным сфигмоманометром и исследуемым прибором средняя разница систолического давления ставила 0,23 мм рт. ст. (p = 0,87), а диастолического – 4,82 мм рт. ст. (p < 0,01).
Ряд технологий измерения АД предполагает получение и анализ пульсовой волны, даже незначительные изменения которой могут предоставить информацию о диагнозе и прогнозе сердечнососудистого заболевания. В настоящее время существует несколько методов неинвазивного безманжетного измерения АД, основанных на регистрации пульсовой волны и имеющих потенциал для применения в клинической практике. К ним относятся фотоплетизмография, механопульсография и устройства, основанные на применении ультразвука.
Метод фотоплетизмографии (ФПГ) основан на определении относительных изменений объема крови в кровеносных сосудах в дерме и подкожной жировой клетчатке. Изменениям объема, вызванным пульсовым давлением, соответствуют изменения поглощения света, который испускается светодиодом и проходит через кожу [13]. ФПГ предоставляет информацию о множестве клинически значимых параметров, таких как насыщение крови кислородом, сердечный ритм, АД, частота дыхательных движений, сердечный выброс, эндотелиальная функция, микроциркуляторный кровоток и функция автономной нервной системы, однако в настоящий момент ее применение ограничено измерением частоты сердечных сокращений и сатурации кислорода в крови [14]. Измерение АД основано на регистрации такого показателя как время распространения пульсовой волны (pulse transit time, PTT), которое рассчитывается как время распространения пульсовой волны из проксимальной точки в дистальную (например, предплечье – палец руки или палец руки – палец ноги) (рис. 4) [15]. Стоит отметить, что некоторые авторы отличают этот показатель от времени прибытия пульсовой волны (pulse arrival time, PAT), которое представляет собой время распространения пульсовой волны от зубца R на ЭКГ до систолической точки на фотоплетизмограмме (рис. 4) [15]. Для получения достоверных сигналов необходима комбинация ФПГ с физиологическими сигналами от дополнительных измерений показателей сердечно-сосудистой системы (ЭКГ, баллистокардиография, фонокардиография), что требует установки на теле нескольких датчиков и, следовательно, затрудняет разработку компактных носимых устройств с использованием этой технологии. Решение этой проблемы было предложено Liu J. и соавт. [14], которые использовали высококомпактную многоволновую ФПГ (highlycompact multi-wavelength photoplethysmography, MWPPG) и метод выделения по глубине (a depth-resolved approach, DRPPG) для продолжительного мониторирования АД. Принцип метода заключается в том, что сигналы от MWPPG несут информацию об изменении объема крови в различных сосудах, а регистрация этих сигналов при помощи волн различных длин и их выделение позволяет реконструировать артериальные, артериолярные и капиллярные пульсовые волны. Малые артерии, расположенные в подкожно-жировой клетчатке, поднимаются в дерму, где делятся на артериолы, и переходят в капилляры на границе эпидермиса и дермы (рис. 5). Поскольку глубина проникновения света зависит от длины волны, то волны, длины которых соответствуют голубому и зеленому цвету, достигают только поверхностно расположенного капиллярного русла, желтый свет способен проникать до артериол, а красный свет и инфракрасное излучение достигают глубоко расположенных артерий (рис. 6). Рисунок 6 демонстрирует алгоритм получения пульсовых волн артерий. Построение пульсовых волн сосудов различного калибра позволяет рассчитать такой показатель как разность времени (depth-resolved time difference – DRPPG TD), определяемый как временной интервал между вершинами реконструированного артериального пульса и капиллярного пульса, полученного при помощи волны, длина которой соответствует голубому свету (рис. 7). DRPPG TD соответствует артериолярному PTT и потому может быть использована для вычисления АД. При этом расчет АД возможен и без реконструирования пульсовой волны по такому показателю, как многоволновая разность времени (multi-wavelength time difference – MWPPG TD), который соответствует временному интервалу между вершинами фотоплетизмограммы с использованием инфракрасного излучения (данный сигнал является комбинацией артериального, артериолярного и капиллярного пульса) и непосредственно капиллярного пульса (рис. 7). Однако значение DRPPG TD составляет около нескольких сотен миллисекунд, тогда как в случае простой MWPPG TD только несколько десятков миллисекунд, то есть последнее в конечном счете ведет к значительно менее точному расчету АД (с полным алгоритмом вычисления АД можно ознакомиться в данной работе). В результате обследования 20 гипертензивных и нормотензивных испытуемых было продемонстрировано, что артериолярный PTT метод с MWPPG позволяет более точно по сравнению с классическим артериальным PTT методом безманжетно измерять АД. Результаты измерений удовлетворяют требованиям AAMI и соответствуют степени А по Стандарту Носимых Безманжетных Устройств для Измерения Кровяного Давления (IEEE Standard for Wearable Cuffless Blood Pressure Measuring Devices, IEEE 1708 Standard). Полноценное исследование данного метода в соответствии с промышленными стандартами потребует большего количества испытуемых. Таким образом, предложенный метод может обеспечить точное измерение параметров сердечно-сосудистой системы, которые обычно сложно измерить неинвазивно и продолжительно. Более того, данный метод позволяет избежать необходимости использовать несколько сенсоров и потому может быть встроен в компактное носимое устройство для комплексного сердечно-сосудистого мониторинга,который включает частоту сердечных сокращений, насыщение крови кислородом, общее периферическое сосудистое сопротивление и АД. Тем не менее, существенными недостатками ФПГ являются недостаточная глубина проникновения, что не позволяет измерять центральное АД, искажение сигналов, чувствительность к теплу и влажности и крайне высокая зависимость от постоянства состава крови [16], поэтому перспективы клинического применения данного метода для измерения АД еще предстоит выяснить.
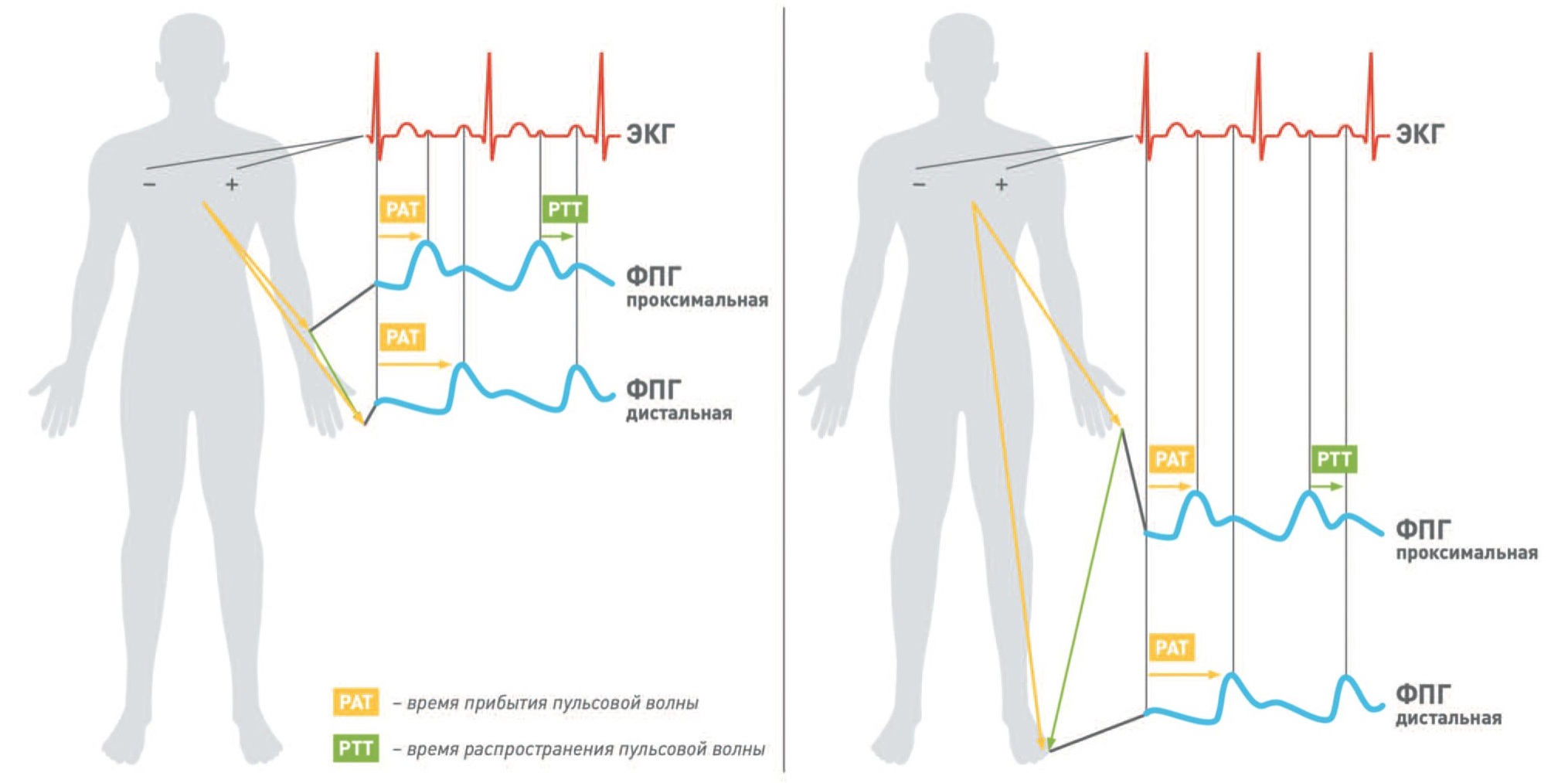
Рис. 4. Различие между временем прибытия пульсовой волны (PAT) и временем распространения пульсовой волны (PTT) ECG – ЭКГ; PPG Proximal – ФПГ проксимальная; PPG Distal – ФПГ дистальная; PAT – время прибытия пульсовой волны; PTT – время распространения пульсовой волны
Fig. 4. Difference between pulse arrival time (PAT) and pulse transit time (PTT) ECG – ECG; PPG Proximal – PPG proximal; PPG Distal – distal FPG; PAT is the arrival time of the pulse wave; PTT – pulse wave propagation time
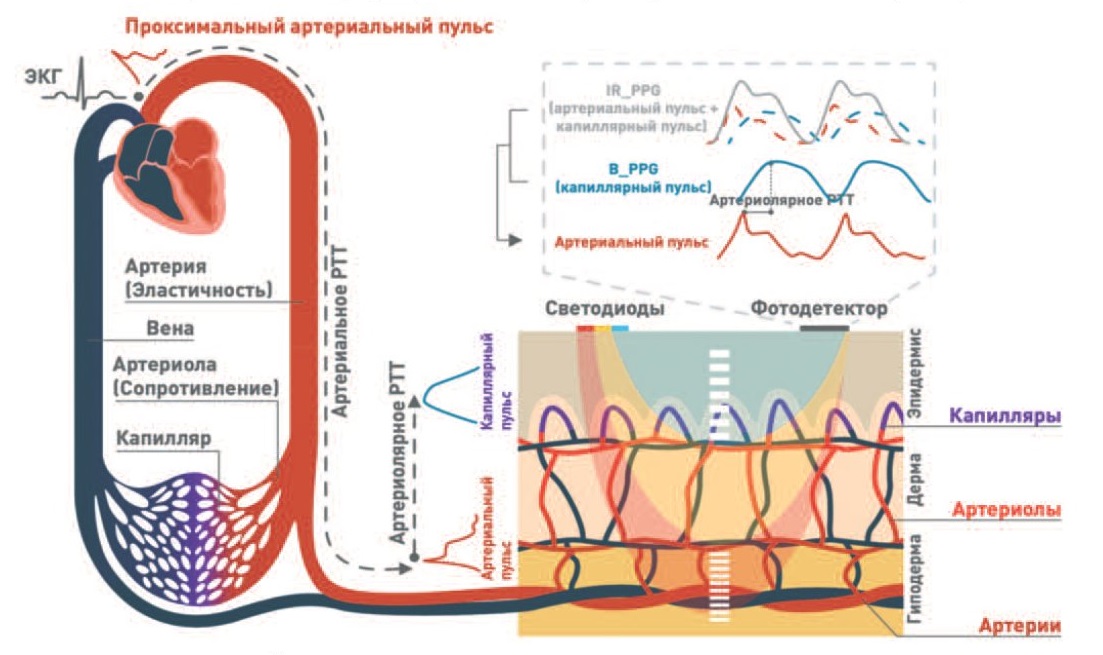
Рис. 5. Системный кровоток и MWPPG IR_PPG (артериальный пульс + артериолярный пульс + капиллярный пульс) – ФПГ с использованием инфракрасного излучения; B_PPG (капиллярный пульс) – ФПГ с использованием волны, длина которой соответствует голубому свету
Fig. 5. The systemic circulation and the MWPPG measurement IR_PPG (arterial pulse + arteriolar pulse + capillary pulse) – PPG using infrared radiation; B_PPG (capillary pulse) – PPG using a wave whose length corresponds to blue light
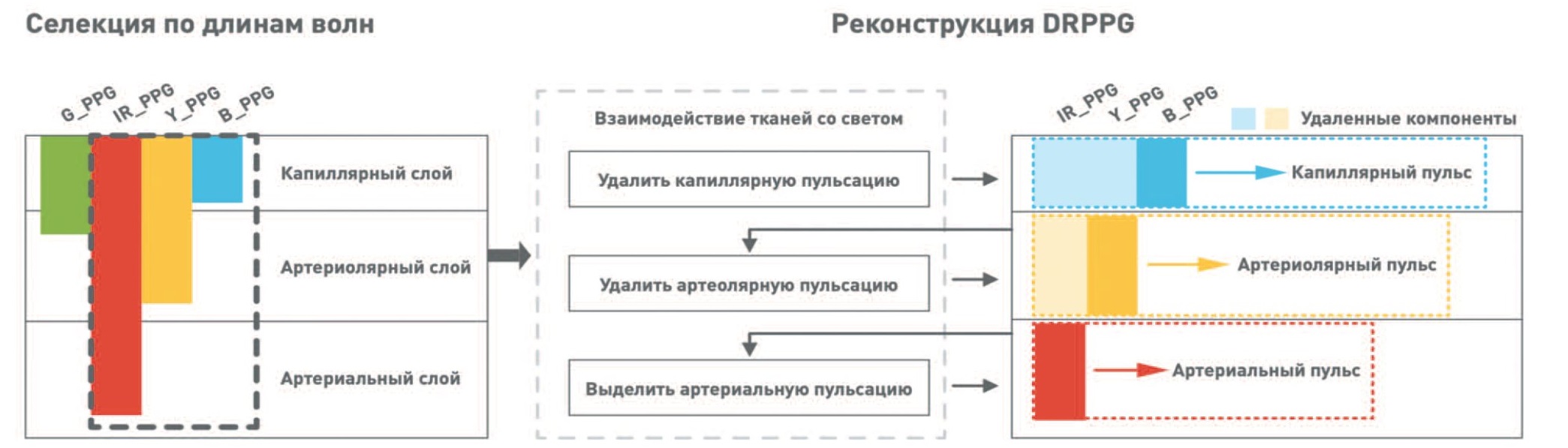
Рис. 6. Реконструкция выделенной по глубине ФПГ из MWPPG G_PPG – ФПГ с использованием волны, длина которой соответствует зеленому свету; IR_PPG – ФПГ с использованием инфракрасного излучения; Y_PPG – ФПГ с использованием волны, длина которой соответствует желтому свету; B_PPG – ФПГ с использованием волны, длина которой соответствует голубому свету
Fig. 6. Reconstruction of DRPPG from MWPPG G_PPG – PPG using a wave whose length corresponds to green light; IR_PPG – PPG using infrared radiation; Y_PPG – PPG using a wave whose length corresponds to yellow light; B_PPG – PPG using a wavelength corresponding to blue light
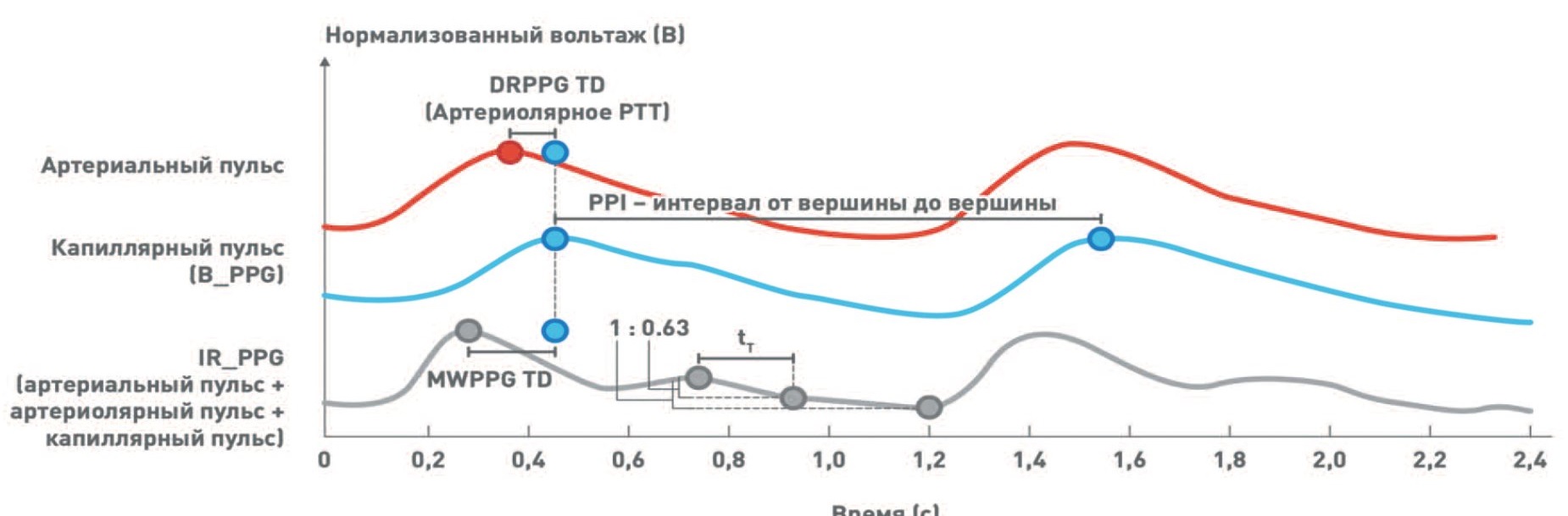
Рис. 7. Получение показателей для вычисления АД. DRPPG TD (Артериолярное PTT) – разность времени (соответствует артериолярному PTT); MWPPG TD – многоволновая разность времени
Fig. 7. Feature extraction for blood pressure estimation DRPPG TD (Arteriolar PTT) – time difference (corresponds to arteriolar PTT); MWPPG TD – Multiwave Time Difference
Другим способом предлагают решить проблему недостаточного объема данных, получаемых с помощью ФПГ и необходимых для вычисления АД, Atomi K. и соавт. Ими был разработан браслет, принцип работы которого основан только на использовании ФПГ [17]. Получение необходимых данных осуществляется при помощи дифференциала второго порядка от пульсовой волны. Данный показатель получил название акселерационной плетизмограммы (acceleration plethysmogram). По отношению всех пиков, содержащихся в полученной волне, к самому первому, а-пику, или а-волне, можно получить информацию о состоянии исследуемого сосуда, в том числе и о жесткости его стенки. Совместно с данными о возрасте, поле, росте и массе тела человека акселерационная плетизмография позволяет получить значение АД. Для исследования точности технологии были сделаны 632 измерения с помощью датчика ФПГ и манжетного тонометра. Стандартное отклонение составило 8,54 мм рт. ст., что согласно критериям Британского общества гипертонии (British Hypertension Society; BHS) соответствует степени B. Изолированное использование ФПГ предлагают и разработчики сенсоров АД без калибровки, которые предназначены для встраивания в носимые устройства, в том числе и в слуховые аппараты [18]. Сенсор такого типа, встроенный в ушное устройство (рис. 9), продемонстриро-вал точность измерений в пределах допустимого отклонения 5 ± 8 мм. рт. ст., что соответствует рекомендациям по сбору данных протокола ISO 81060-2:2018.
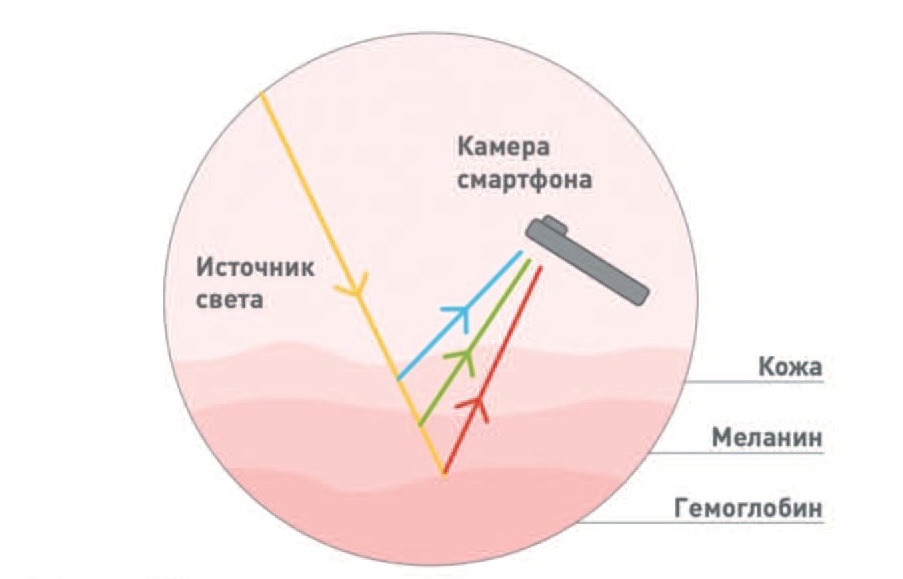
Рис. 8. Метод TOI, в котором свет видимого спектра проходит через поверхность кожи и отражается, а затем фиксируется камерой смартфона. Далее фиксируются малозаметные изменения в цвете кожи, из-за разницы в отраженном свете между гемоглобином и меланином, благодаря чему определяется поток крови в сердечно-сосудистой системе
Fig. 8. TOI technology. Light from the visible spectrum travels through skin surface, re-emits, and then becomes captured by smartphone’s camera. Then subtle changes in skin color caused by the difference in re-emitted light between hemoglobin and melanin are used to detect blood flow in cardiovascular system
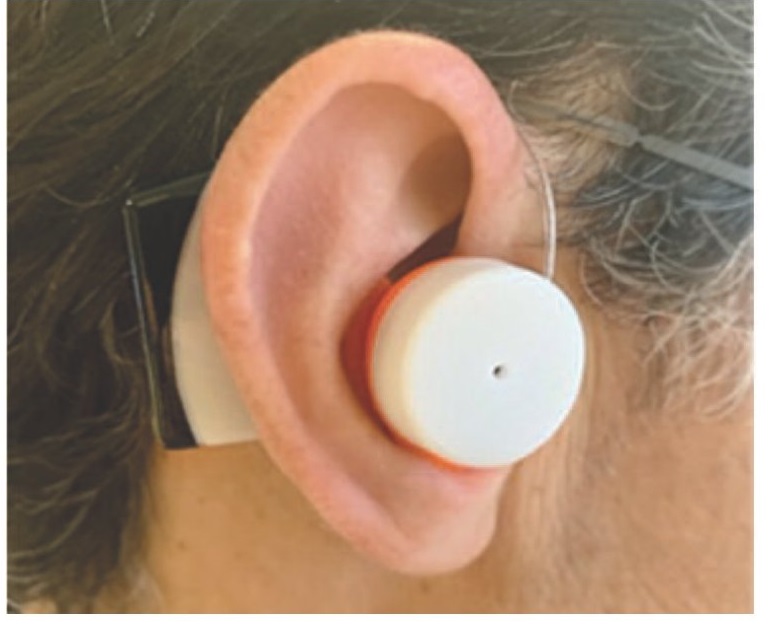
Рис. 9. Сенсор, встроенный в ушное устройство
Fig. 9. Sensor integrated in hearing aids
Для получения фотоплетизмограммы Luo H. и соавт. предложили использование камеры смартфона и машинное обучение [19]. Данный метод называется трансдермальная оптическая обработка изображения (transdermal optical imaging, TOI). Каждый кадр видео, снятого на телефон, разделяется на слои, содержащие по три цветовых канала. Камера телефона фиксирует отраженный от кожи свет, который определяется уровнем гемоглобина в крови и меланином в коже человека (рис. 8). В каждом кадре выделяются сигналы, которые содержат информацию о концентрации гемоглобина на определенном участке кожи. Таким образом, получается видео, показывающее изменяющуюся концентрацию гемоглобина. Предполагается, что TOI измеряет частоту сердцебиения с точностью ЭКГ, и вариабельность сердечного ритма, так как эти параметры определяются по току крови. Считывание информации с 17 зон на лице человека, находящихся на лбу, носу, щеках, губах, подбородке, а также губном желобке, позволяет получить более точные данные об уровне АД, в отличие от привычного метода измерения с помощью ФПГ на пальце. В исследовании технологии приняли участие 2348 человек с нормальным АД, данные собирались в течение 2 лет. Точность измерений составила 94,81% для систолического АД и 95,71% для диастолического, а средняя погрешность составила от 6 до 7,30 мм рт. ст. Таким образом, результаты соответствуют стандартам AAMI, однако дальнейшая валидация технологии требует исследования на испытуемых не только с нормальным, но и с повышенным и пониженным АД.
Многие разработчики предлагают использовать ФПГ совместно с другими методами измерения, что увеличивает точность измерений. Например, в 2017 году был создан браслет, принцип работы которого основан на ФПГ и сейсмокардиографии [20]. Сейсмокардиография – это метод измерения вибраций грудной клетки, вызванных сердцебиением [21]. Браслет, получивший название SeismoWatch, позволяет вычислять PTT благодаря встроенному в него акселерометру. Браслет, приложенный к грудине на короткое время (около 15 секунд), регистрирует колебания грудной клетки, связанные с сердечными сокращениями.
Эти данные позволяют получить информацию о проксимальной точке, и совместно с данными о дистальной точке при измерении с помощью ФПГ на запястье вычислить PTT, на основании которого рассчитывается АД. Данный метод является относительно простым решением за счет акселерометра, однако, как указано авторами, требует периодической калибровки. После калибровки погрешность в измерениях составляет менее 5 мм рт. ст. более чем в 95% случаев. Другое решение представляет собой носимый монитор для продолжительного измерения систолического АД, который включает радар непрерывного действия, размещенный на грудине и регистрирующий расширения вентральной поверхности при колебаниях аортального клапана, датчик ФПГ на левой мочке уха и электроды ЭКГ на груди (рис. 10) [22]. Систолическое АД рассчитывается после измерения и математической обработки PTT, PAT и периода изоволюмического сокращения (pre-ejection period – PEP). PEP определяется как интервал между отрезком сигнала радара и R-зубцом на ЭКГ либо извлекается из PAT при получении сигнала ФПГ. Измерение АД проводилось на 43 добровольцах, при этом точность у тех, кто выполнял задачи по изменению положения тела составляла 92,28%, а у участников исследования, выполнявших физические упражнения – 82,61%. Необходимо отметить, что при выделении PEP из PAT точность результатов улучшалась приблизительно на 9%.
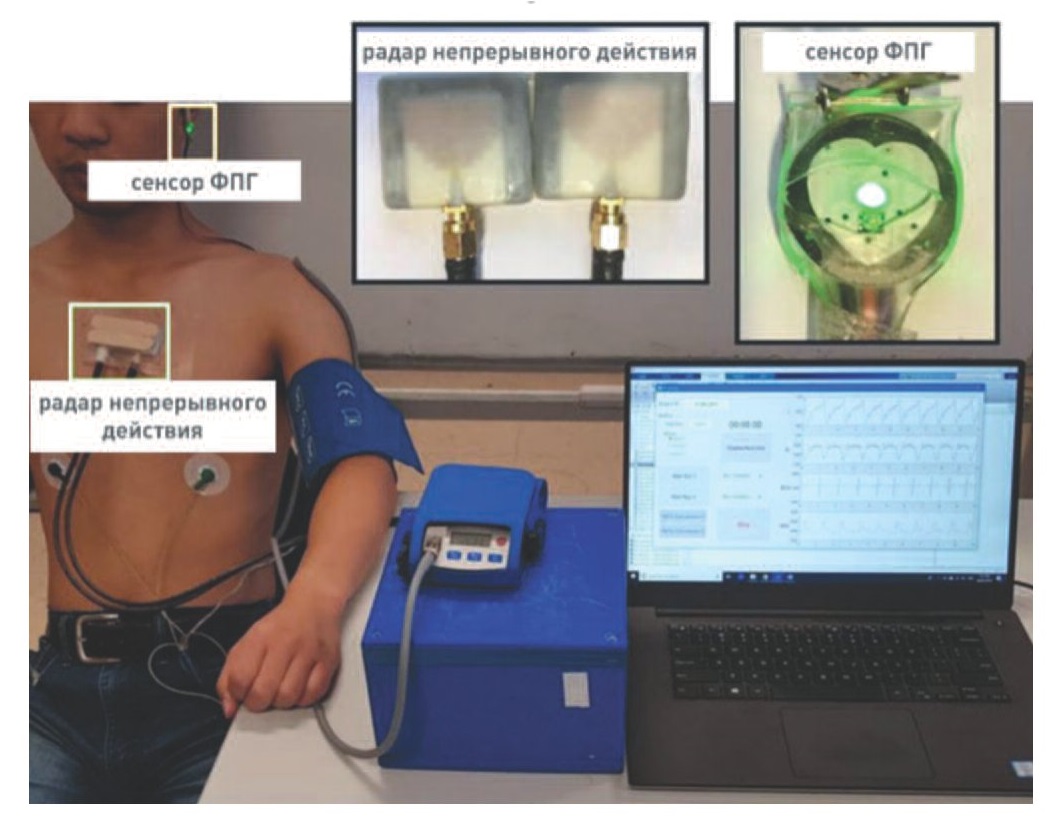
Рис. 10. Размещение радара непрерывного действия, ЭКГ и ФПГ сенсоров на обследуемом, сидящем на велоэргометре
Fig. 10. The placement of сontinuous wave radar, ECG and PPG sensors on a participant seated on an exercise bike
По мнению некоторых авторов, перспективной технологией для продолжительного измерения АД является баллистокардиография (БКГ). В одной из первых статей о БКГ, опубликованной в 1967 году, указано, что данный метод основан на использовании двух платформ, которые имеют высокую и низкую частоту колебания. Запись отклонений данных платформ отражает колебания тела человека, связанные с сердцебиением и током крови [23]. Более точно было установлено, что движения тела, регистрируемые при измерении с помощью БКГ, обусловлены выбросом крови из сердца в сосудистую сеть [21]. Вычисление АД основано на анализе баллистокардиограммы. Например, из волны, полученной при измерении методом БКГ, были выделены пики (I, J, K), по интервалам между которыми возможно определение диастолического давления. Амплитуда двух других пиков позволяет определять пульсовое давление [24]. Исследование прибора было проведено на 22 участниках, и измерения проводились пятью различными методами: пластиной, измеряющей АД с помощью БКГ; встроенным в эту пластину датчиком ФПГ, снимающим фотоплетизмограмму на стопе; электродами для снятия ЭКГ; зажимом на палец с датчиком ФПГ и манжетой на среднем пальце для снятия ФПГ. В результате было показано, что интервал I-J совместно c амплитудой J-K позволит проводить точное мониторирование систолического и диастолического АД с помощью БКГ. Точность измерений составила 8 мм рт. ст. для диастолического давления и 12 мм рт. ст. для систолического, что сравнимо с измерением аускультативным способом. Однако неудобством данного метода является использование пластины, которая препятствует постоянному мониторингу АД, и требует специальных условий для проведения измерений. Решение данной проблемы было найдено в исследовании Lee K. и соавт. [25]. В данной работе для измерения АД методом БКГ используется двухканальный датчик. Вычисляемая по уравнению Гилберта разница между двумя одновременными сигналами с помощью нейронной сети позволяет получить показатели АД. Данный метод получил название метода мгновенной разности фаз (instantaneous phase difference, IPD). Устройство с применением данной технологии представлено в виде стула, в спинке и сиденье которого находятся сенсоры из поливинилиденфторида (PVDF), прикрепленные на слой уретановой пены, а поверх сенсоров прибор покрыт натуральной кожей. Авторы предложили использовать такой метод для постоянного мониторинга АД, поскольку датчики могут быть встроены в любой стул. Исследование было проведено на 30 участниках с нормальным АД. Количество испытуемых и низкая точность части измерений не соответствовали требованиям AAMI.
Еще одной многообещающей технологией является ультразвуковое исследование, применение которого для регистрации показателей сердечнососудистой системы берет начало в 2011 году [26]. По сравнению с ФПГ приборы, основанные на применении ультразвука, обладают более высокой проникающей способностью и позволяют исследовать параметры кровотока на глубине до 4 см [16]. Это предоставляет возможность измерять центральное АД, которое более информативно в диагностике и контроле течения сердечно-сосудистых заболеваний, чем периферическое АД. Вместе с тем клиническое применение данного метода ограничено рядом причин, среди которых высокая чувствительность к двигательным артефактам, громоздкость самого датчика, необходимость использования геля [27]. Для обеспечения достоверной акустической связи необходимо стабилизировать датчик, что оказывает влияние на расположенные вблизи сосуды и тем самым снижает точность регистрируемых сигналов. Перспективным в преодолении данных недостатков является носимый эластичный ультразвуковой прибор, прикрепляющийся к коже и позволяющий регистрировать пульсовые волны в глубоко расположенных артериях и венах [16]. Еще в 2016 году Kim I. и соавт. был разработан портативный импульсно-волновой доплер с низким потреблением мощности и дизайном, позволяющим поместить его в носимое устройство [27].
Модель Wang и соавт. создана в формате ультратонкого и растяжимого патча и предоставляет возможность для неинвазивного, длительного и точного мониторирования состояния сердечно-сосудистой системы из различных областей тела [16]. Принцип работы данного прибора основан на непрерывной регистрации диаметра пульсирующего сосуда при помощи пьезоэлектрического датчика, который преобразует электрический потенциал между верхними и нижними электродами в механические вибрации и наоборот. Электроды располагаются в соответствии с локализацией сосудов, что позволяет избежать трудоемкой ручной установки. Дизайн прибора обеспечивает эффективную глубину проникновения при минимальной механической нагрузке на кожу. Снаружи прибор покрыт силиконовым эластомером, гидрофобные свойства которого обеспечивают защиту от влажности и возможной коррозии от пота. Тонкий слой силикона избавляет от необходимости использования геля. Вместе с тем прибор способен выдерживать скручивание и растягивание, что свидетельствует о его высоком потенциале для фиксации на коже. Таким образом, эластомерный матрикс с многозвенным растягивающимся дизайном и ультратонкой капсулой обеспечивает исключительно плотный и плавный контакт с кожей человека при различных видах деформации, а технические характеристики позволяют осуществлять высокоточное измерение пульсирующего характера центральных сосудов (внутренняя сонная артерия, внутренняя и наружная яремные вены).
Проверка функциональных свойств прибора проводилась на мужчине 22 лет с нормальным АД в положении сидя посредством сопоставления с показаниями коммерческого прибора – золотого стандарта для регистрации пульсовой волны, одобренного FDA (тонометр SphygmoCor EM3). Последний должен фиксироваться на запястье оператором (исследователем), что оказывает значительное давление (~100 Па) на кожу и вызывает сильное раздражение. Более того, это давление искажает сигнал и ведет к ошибочному считыванию. В отличие от него, прибор, основанный на применении ультразвука, непосредственно прикрепляется к коже и оказывает минимальное давление (~5 Па) из-за сверхлегкой массы (0,15г), что обеспечивает не только возможность длительного мониторирования без какого-либо дискомфорта для испытуемого, но и относительно стабильную и продолжительную регистрацию показателей даже во время движения. Таким образом, прибор, основанный на применении ультразвука, обладает меньшей относительной погрешностью измерения (1%), большей точностью регистрации АД (в пределах 2 мм рт. ст.) и более высокой точностью измерения (степень A в соответствии с критериями BHS, а также соответствует стандарту AAMI SP10), чем коммерческий прибор. Прибор Wang и соавт. может внести особый вклад в понимание характеристик центрального венозного и центрального АД путем непрерывного мониторирования, но необходима его валидация с инвазивным методом измерения АД и, что наиболее важно, в условиях реальной клинической практики. Необходимо понять, какие движения тела и шеи допустимы перед тем, как произойдет искажение сигнала.
Более того, любая технология, которая требует первоначальной калибровки с манжетой и условия, что диастолическое давление остается неизменным в течение времени мониторирования, что характерно и для данного прибора, ограничит ее применение у пациентов при угрозе резкого снижения общего периферического сосудистого сопротивления [1].
Еще одной перспективной технологией при разработке приборов для неинвазивного непрерывного АД является метод регистрации пульсовой волны, относящийся к механопульсографии [28]. Принцип действия волоконно-оптических датчиков, преобразующих колебания артериальной стенки, заключается в моделировании светового потока за счет колебаний металлической мембраны синхронно с колебаниями сосудистой стенки. На основе данных датчиков могут быть разработаны устройства, помещаемые на запястье руки, для измерения АД с клинической точностью.
Интересным решением является использование электронных тату (e-tattoos). Одно из таких устройств, разработанное Ha T. и соавт., основано на применении сейсмокардиографии [29]. Данное устройство представляет собой ультратонкий сенсор (толщина составляет 28 микрометров) из сети змеевидных нитей из поливинилиденфторида с меде-никелевыми электродами, расположенными наверху и внизу. Змеевидная форма частей сенсора обеспечивает растяжимость при ношении, что позволяет преодолеть проблему нерастяжимых пьезоэлектрических мембран, применяемых в сейсмокардиографии. Кроме того, особенности выбранного субстрата наделяют прибор способностью подстраиваться под деформации кожи при движениях. В виду того, что на данном этапе нет единого мнения о месте наиболее точного снятия сейсмокардиографии, наиболее подходящее местоположение сенсора было определено с помощью метода 3D корреляции цифровых изображений (3D digital image correlation, 3D DIC) и акселерометра. Технология 3D DIC позволяет с помощью камер определить деформацию, растяжение и другие характеристики исследуемого объекта [30]. Для этого сразу 3 сенсора были прикреплены в различных местах грудной клетки. Ее движения были засняты высокоскоростной камерой, расположенной под углом в 30 градусов относительно грудной клетки. Измеренные таким образом изменения грудной клетки при дыхании и сердцебиении были разделены на области и обозначены различными цветами, в зависимости от соответствия пиков звука и изменения поверхности (в микрометрах). Таким образом было выяснено, что наиболее точным будет измерение с помощью 2 сенсоров, расположенных в 1 см друг от друга (рис. 11).
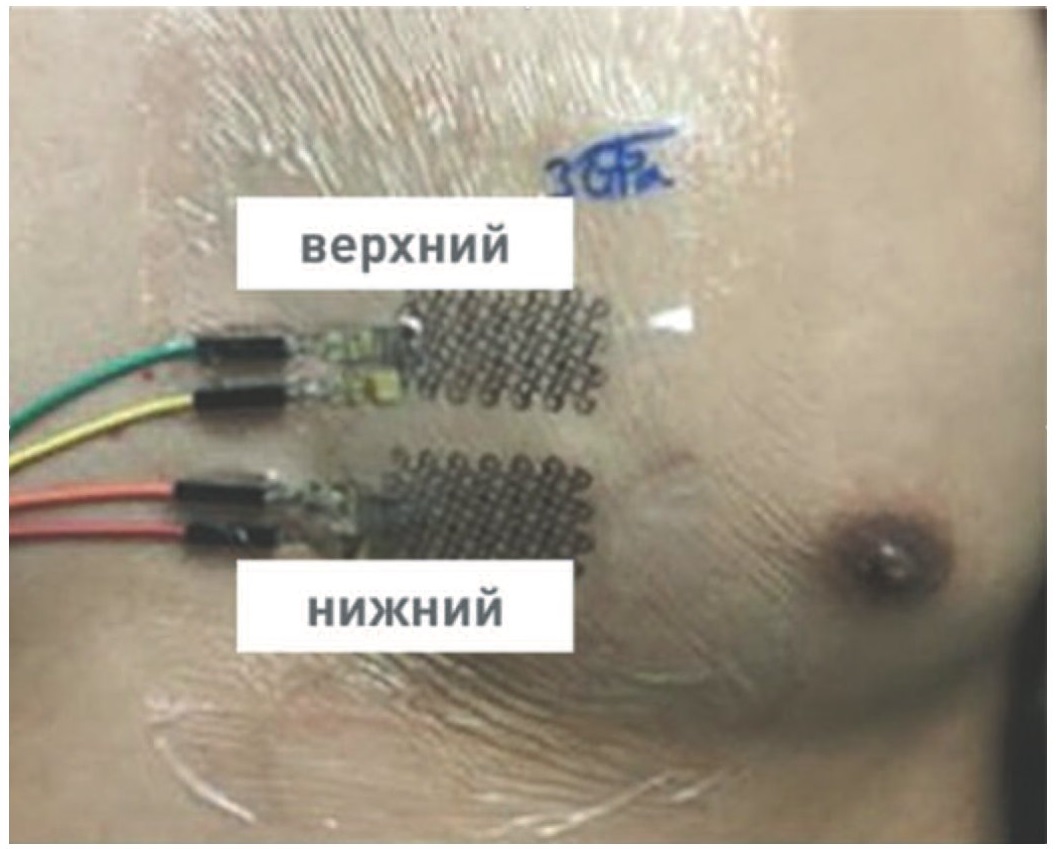
Рис. 11. Наиболее эффективное для измерения АД положение тату-датчиков на теле
Fig. 11. The most effective location of E-tattoo for measuring blood pressure
Медицинская значимость e-tattoo повышается при применении сенсора совместно с сенсором ЭКГ (рис. 12). В таком случае получается электрокардио-акустический сердечно-сосудистый сенсор, позволяющий измерять АД. Его размеры составляют 63,5 мм х 38,1 мм х 0,122 мм, масса 150 мг, и благодаря 100% растяжимости на данный момент такой сенсор не имеет аналогов. С помощью ЭКГ снимаются P, Q, R, S, T зубцы, а с помощью сейсмокардиографии регистрируются пики, соответствующие открытию аортального клапана, его закрытию и открытию митрального клапана. Корреляции между пиками ЭКГ и сейсмокардиографии позволяют найти интервалы между R-зубцом и пиком закрытия аортального клапана, что соответствует систоле и позволяет вычислить систолическое и диастолическое давление.
Невыясненным вопросом остается точность показаний разрабатываемых неинвазивных безманжетных приборов в условиях активных движений пациентов. Преодолеть данную проблему представляется возможным в случае применения минимально-имплантируемых приборов [31–34], которые измеряют АД на артерии экстраваскулярно.
Принципиально новый подход для измерения АД – импедансная плетизмография, используется в работе [35], где осуществляется измерение сосудистого сопротивления путем регистрации растяжения стенки кровеносного сосуда. Прибор состоит из четырех плоских 10 мм2 медных электродов на подложке из гибкой полиимидной пленки с подковообразными структурами (рис. 13). Для исследования ex vivo система была помещена на сонную артерию домашней свиньи в искусственной системе кровообращения (рис. 14). In vivo прибор был проверен на домашней свинье (самец, шесть месяцев, масса тела 103 кг) во время операции, в ходе которой четыре электрода были расположены на бедренной артерии (рис. 15). Результаты измерений показали высокую корреляцию с показателями АД. После калибровки системы производительность датчика достигает самого высокого уровня измерения кровяного давления согласно критериям BHS, что соответствует степени А. Метод является перспективным в оценке внутреннего диаметра артерии как показателя динамики развития артериосклероза.
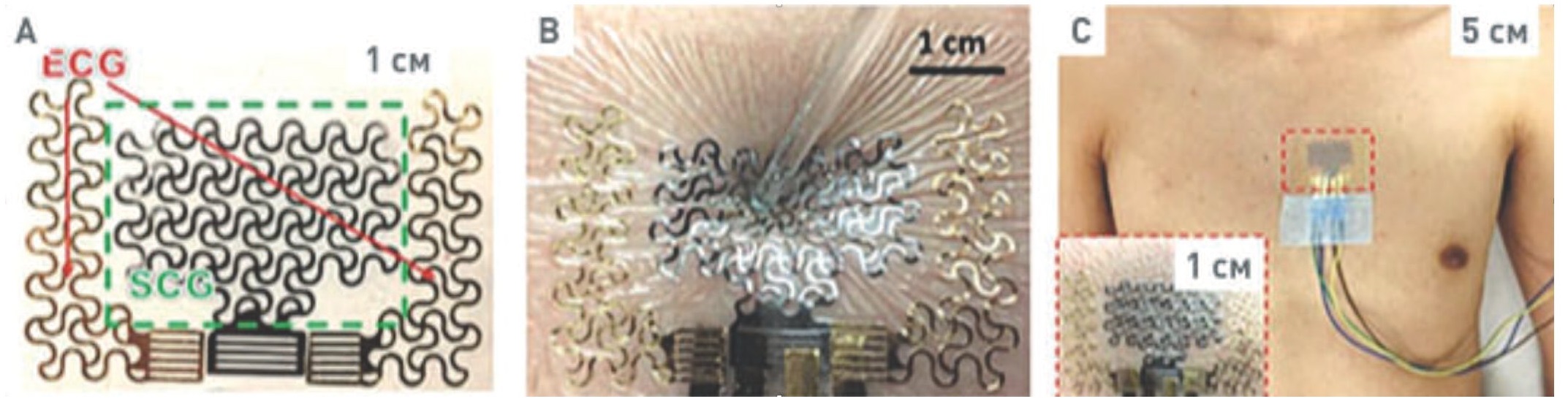
Рис. 12 А. Сенсор сейсмокардиографии (в центре) и ЭКГ (по периметру). B. Тату-подобная деформация сенсора. C. Фотография сенсора с подключенными проводами на грудине человека
Fig. 12. A. Seismocardiograhy sensor (in the center) and ECG (on the borders of E-tattoo). B. Tattoo-like deformation of the sensor. C. A picture of the sensor on human chest with connected wires
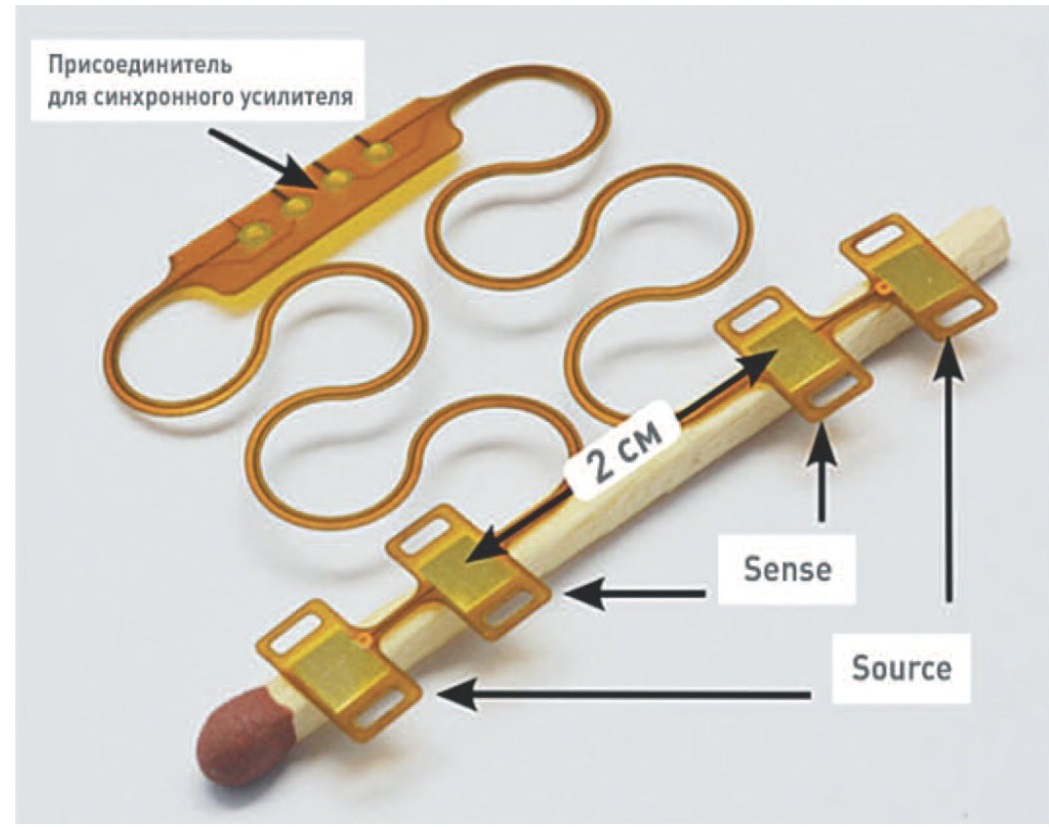
Рис. 13. Гибкая полиимидная пленка с четырьмя электродами, которые накладываются на артерию
Fig. 13. Flexible polyimide foil with four electrodes to be placed on an artery

Рис. 14. Исследование устройства импедансной плетизмографии ex vivo. Электроды помещены на сонную артерию домашней свиньи в искусственной системе кровообращения при помощи силиконовых полосок.
Fig. 14. Setup of the ex vivo measurement with a carotid artery of a domestic pig in an artificial circulatory system. The IPG electrodes are placed on the artery by means of flexible silicone strips
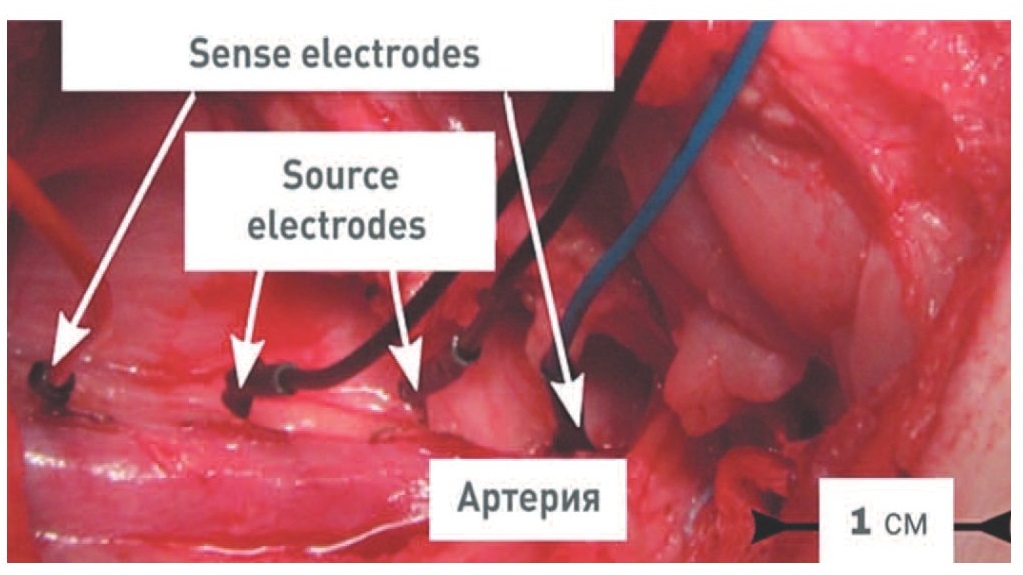
Рис. 15. Исследование устройства импедансной плетизмографии in vivo. Электроды импедансной плетизмографии расположены на бедренной артерии домашней свиньи.
Fig. 15. Setup of the in vivo measurement with a femoral artery of a domestic pig
Среди имплантируемых датчиков аналогом импедансной плетизмографии является сенсор, в основе работы которого лежит деформация мембраны и изменение ее емкости за счет механического давления артерии [36, 37]. Кроме точности измерений, достоинством этого сенсора является отсутствие батареи, так как он является сенсором пассивного типа, способным функционировать без использования источников питания. Для проверки свойств прибора проводились исследования прочности датчика с помощью термического акселерационного теста, а также in vitro совместимости с организмом. Исследование точности измерения АД проводилось на животных.
Аналогичным, но не имплантируемым сенсором, является датчик, предназначенный для измерения АД на лучевой артерии [38]. В данном сенсоре используется технология микроэлектромеханических систем (microelectromechanical systems, MEMS), позволяющая значительно уменьшить размеры датчика. Диафрагма датчика, сделанная из силикона, располагается над лучевой артерией и регистрирует изменения давления за счет пульсации артерии. Данное устройство не может предоставить данные об абсолютном значении АД, и потому требует калибровки с помощью обычного сфигмоманометра перед началом использования. В исследовании прибора приняли участие 92 добровольца, давление которых измерялось с помощью сфигмоманометра и описанного устройства. После 20 минут измерений датчик показал значительные отклонения от значений сфигмоманометра. Однако измерение давления у пациентов, находящихся под анестезией и во время операции, показало результаты, аналогичные инвазивному измерению АД. Таким образом, недостатком данного датчика является необходимость неподвижного положения пациента при измерении, в связи с чем Satake S. и соавт. предлагают применять этот прибор у пациентов, находящихся без сознания (например, во время операций вместо инвазивных способов измерения АД).
Подобный недостаток отсутствует у датчика, измеряющего давление на сонной артерии при помощи купола, заполненного воздухом [39]. Вибрации артерии приводят к деформации нижней части устройства, и, соответственно, увеличению плотности воздуха внутри купола. Данные изменения фиксируются датчиком и, таким образом, позволяют получить пульсовую волну. Использование такого куполообразного датчика совместно с ЭКГ позволяет определять не только АД, но и вариабельность сердечного ритма по R зубцу из электрокардиограммы, а также трем основным пикам пульсовой волны. Исследования прибора проводились на 5 добровольцах, поэтому дальнейшая валидация прибора как медицинского устройства, в первую очередь, требует большего числа испытуемых, в том числе с отклонениями от нормального уровня АД.
Canning и соавт. предлагают измерение АД на поверхностной височной артерии [40]. Выбор артерии связан с ее расположением: в вертикальном положении тела голова расположена над сердцем, что позволяет найти связь давления в ней с давлением в аорте. Внешне прибор выглядит как компьютерные наушники. В правой части прибора находится шаговый мотор и пьезорезистентный датчик давления, который генерирует пульсирующие сигналы разной частоты. Среди них выделяются сигналы высокой и низкой частоты, по которым происходит вычисление АД после калибровки прибора манжетным тонометром. Исследование точности проводились с помощью манжетного тонометра, а также устройства Nexfin, имеющего одобрение FDA. Полученные прибором данные отличались от стандарта на 7,7% (примерно 7 мм рт. ст.), в то время как данные Nexfin – на 7,3%, что говорит о его достаточно высокой точности.
Кроме того, существуют множество приборов, созданных для постоянного мониторинга давления при определенных заболеваниях. Например, Kamijo Y. и соавт. предлагают мониторинг АД у пациентов, находящихся на гемодиализе. С помощью специально созданного электронного стетоскопа получают данные об интенсивности тока в артериально-венозной фистуле, которые затем преобразовываются с помощью метода Фурье [41]. В исследовании приняли участие 26 пациентов, находящихся на гемодиализе, и всего было проведено 315 измерений. Стандартная ошибка измерения составила 5,8 мм рт. ст., что является показателем высокой точности прибора. Перспективным считается применение данного метода для выявления интрадиализной гипотонии, которая является серьезным осложнением у пациентов на гемодиализе [42].
ОБСУЖДЕНИЕ
Выполненный в ходе работы анализ литературы позволяет классифицировать существующие приборы для неинвазивного измерения АД в соответствии с двумя критериями.
В первом случае классификация может быть представлена следующим образом (рис. 16):
Классификация приборов (по мобильности)
1) Немобильные (стационарные) приборы
- a) Стационарные автоматические тонометры
2) Переносные приборы
- a) Автоматические манжетные тонометры
- b) Приборы, основанные на методе баллистокардиографии
3) Носимые приборы
- a) Браслеты
- b) Манжетки на палец
- c) Головные уборы (наушники)
- d) Смартфоны и т. д.
4) Прикрепляемые сенсоры
- a) Тату
- b) Патчи
5) Имплантируемые датчики
- a) Экстраваскулярные
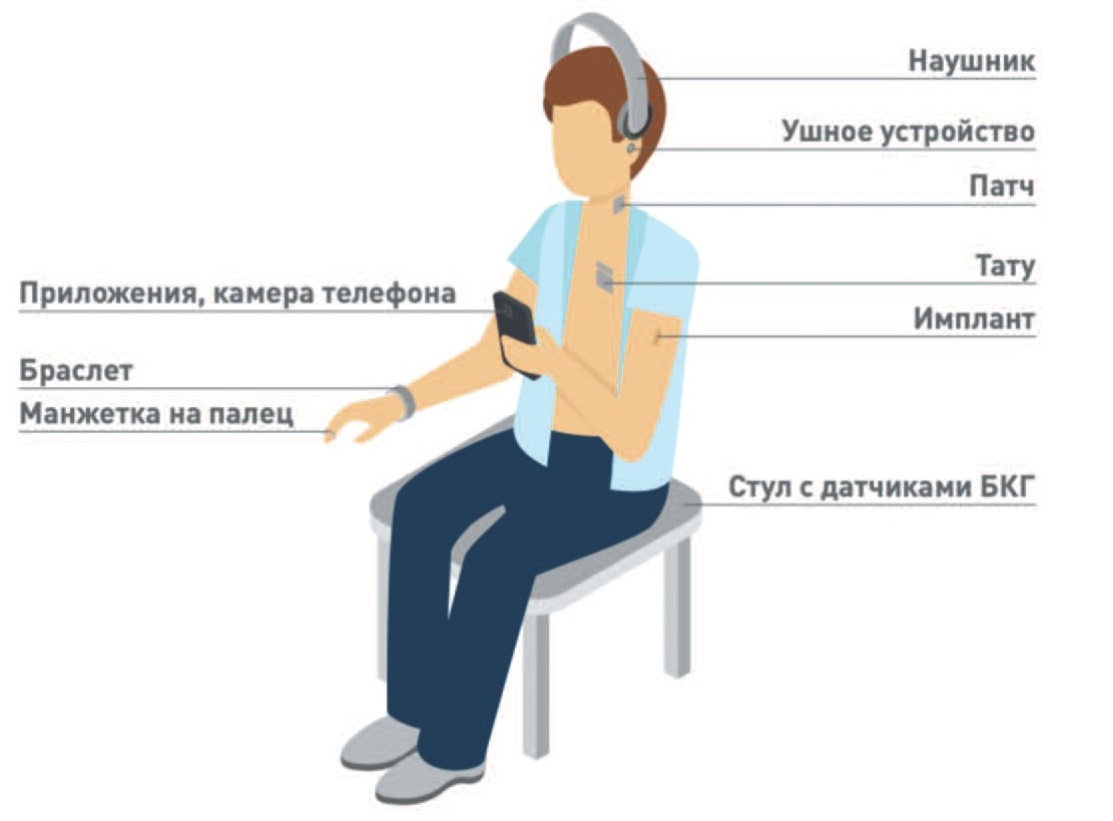
Рис.16. Классификация приборов для мониторинга АД в повседневной жизни.
Fig. 16. Classification of devices for blood pressure estimation used in daily life
Во-первых, все приборы могут быть разделены по их мобильности. Внутри нее можно выделить несколько групп.
К первой группе будут относиться немобильные, стационарные приборы, размер и вес которых не позволяет использовать их вне специализированных помещений. К ним относятся стационарные автоматические тонометры [43].
Вторая группа включает в себя переносные приборы, которые возможно брать с собой, но они не могут быть использованы для продолжительного мониторинга в силу громоздкости. К ним относятся наиболее распространенные в настоящее время автоматические манжетные тонометры и приборы, основанные на методе баллистокардиографии, поскольку оба варианта представляют собой устройства, неудобные для использования при активном образе жизни.
Третья группа объединяет носимые приборы, разнообразие которых значительно больше. Чаще всего такие приборы подразумевают постоянное ношение на теле, и потому они отличаются небольшими размерами и массой для удобства их использования. Наиболее популярными являются браслеты, предназначенные для ношения на запястье и часто включающие в себя, помимо измерения АД, большое количество других функций (счет шагов, отображение времени и т.д.). Однако можно встретить и такие варианты, как манжетки на палец, головные уборы со встроенными датчиками и даже смартфоны, функциональные особенности которых некоторые исследователи предлагают использовать для измерения АД.
В четвертую группу следует выделить патчи и тату, поскольку разработка таких устройств требует других технологий и методов, в отличие от привычных и более распространенных браслетов. Прикрепление этих приборов возможно на любой участок кожи, что позволяет использовать для измерения АД не только плечевую и лучевую артерию, но также и другие сосуды, что предоставляет возможности для получения более точных показаний.
И пятая группа включает имплантируемые датчики, которые чаще всего прикрепляются к наружной части артерии или другого сосуда, и имеют ряд преимуществ (малый размер, непрерывный мониторинг в течение всего срока ношения, низкое потребление энергии) относительно других носимых приборов для измерения АД.
Во-вторых, все существующие методы можно разделить по технологии измерения АД. «Золотым стандартом» среди неинвазивных методов принято считать измерение по тонам Короткова. Получаемые таким методом данные не требуют специальной обработки, поскольку тоны Короткова можно прослушать с помощью стетоскопа. Кроме него, распространен и осциллометрический метод, измерения давления в котором происходит за счет регистрации колебаний воздуха в манжете. Автоматические манжетные тонометры на данном этапе наиболее распространены для «домашнего» измерения АД.
К методам измерения АД, основанным на анализе колебаний стенок артерий, относятся фотоплетизмография и механопульсография. Поскольку данные, получаемые с помощью ФПГ, не позволяют сразу определить уровень АД, требуется их дополнительная математическая обработка, либо использование нескольких источников снимаемой волны. Недостаточное количество информации, получаемое с помощью ФПГ, приводит к тому, что часто данную технологию используют совместно с другими методами, например, с ЭКГ, акселерометрами и т.д. В виду этого приборы, основанные на применении ФПГ с другими методами, можно объединить в одну группу.
К последующим группам относятся УЗИ, импедансометрия и другие технологии, которые используются гораздо реже, в отличие от трех первых групп.
Наконец, при разработке прибора важно учитывать цели его дальнейшего применения. Мониторинг подразумевает под собой как отслеживание показателей состояния здоровья при активном образе жизни, так и их контроль при стационарном лечении или во время операций. На данный момент для мониторинга АД при проведении операций используют катетеризацию сосуда, которую в перспективе можно заменить неинвазивными приборами, более комфортными для пациента. Часть технологий показывает гораздо более точные результаты при измерении в покое, а не при активном движении, что делает их перспективными для использования в стационарах. Использование в условиях активного образа жизни предполагает другие требования к прибору. Например, становится важным точность измерений при движении, либо возможность прибора подстраиваться под человека и осуществлять измерения в подходящие промежутки времени. Существующие на данный момент приборы во многом пока еще далеки от соответствия требованиям к приборам для мониторинга АД при активном образе жизни, поскольку теряют свою точность при измерении в движении. В связи с этим становится важным дальнейшее развитие технологий и усовершенствование устройств для использования в повседневной деятельности.
Следует отметить, что новые устройства измерения АД будут не способны самостоятельно анализировать всю считываемую информацию в связи с тем, что в процессе работы осуществляется регистрация изменений на протяжении длительного периода времени, а также отслеживание корреляции показателей АД с другими параметрами. Результатом этого станет получение огромного массива данных, анализ которого будет затруднен в том числе и для врача, что свидетельствует о необходимости разработки системы их обработки и программного обеспечения.
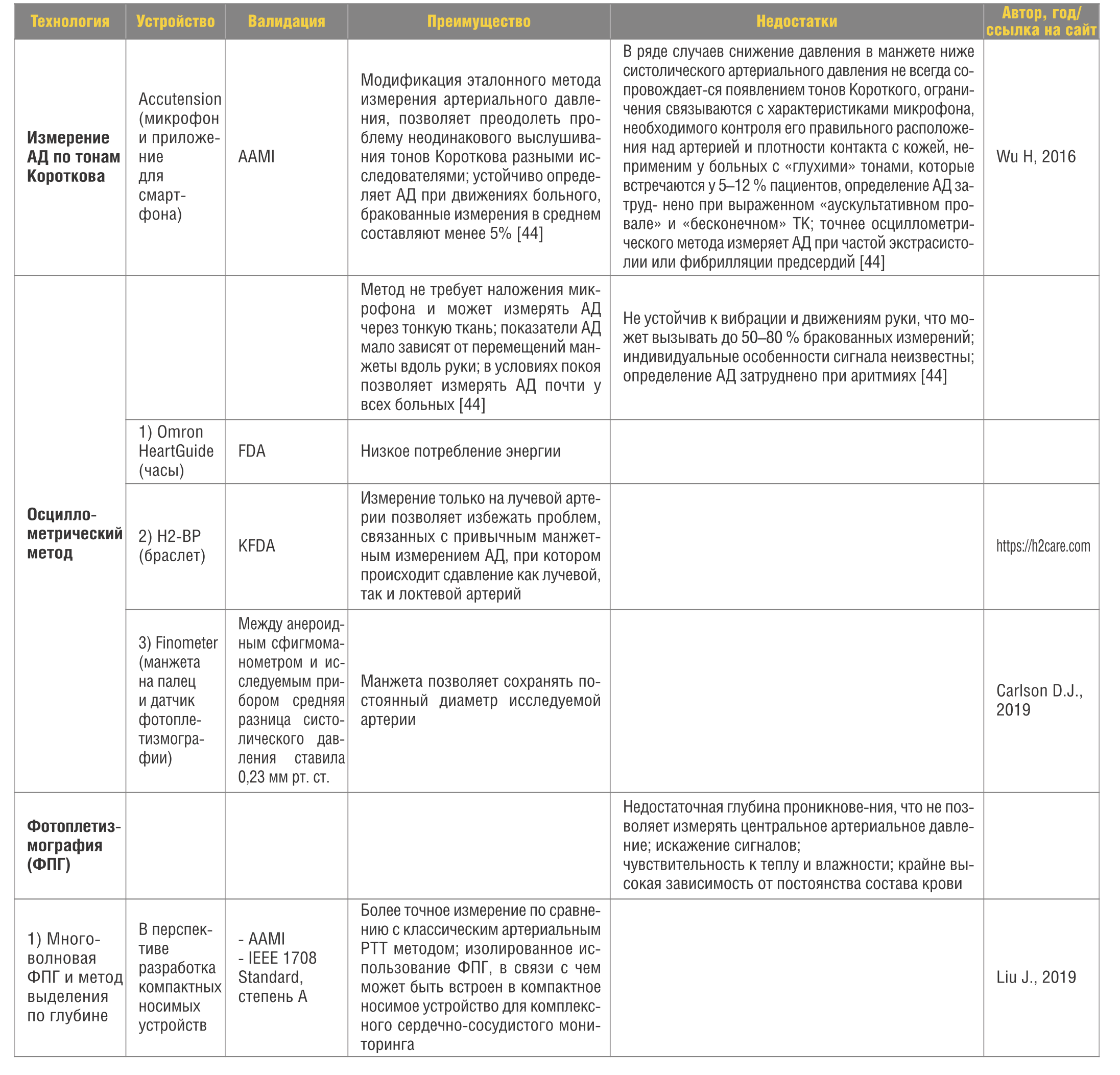
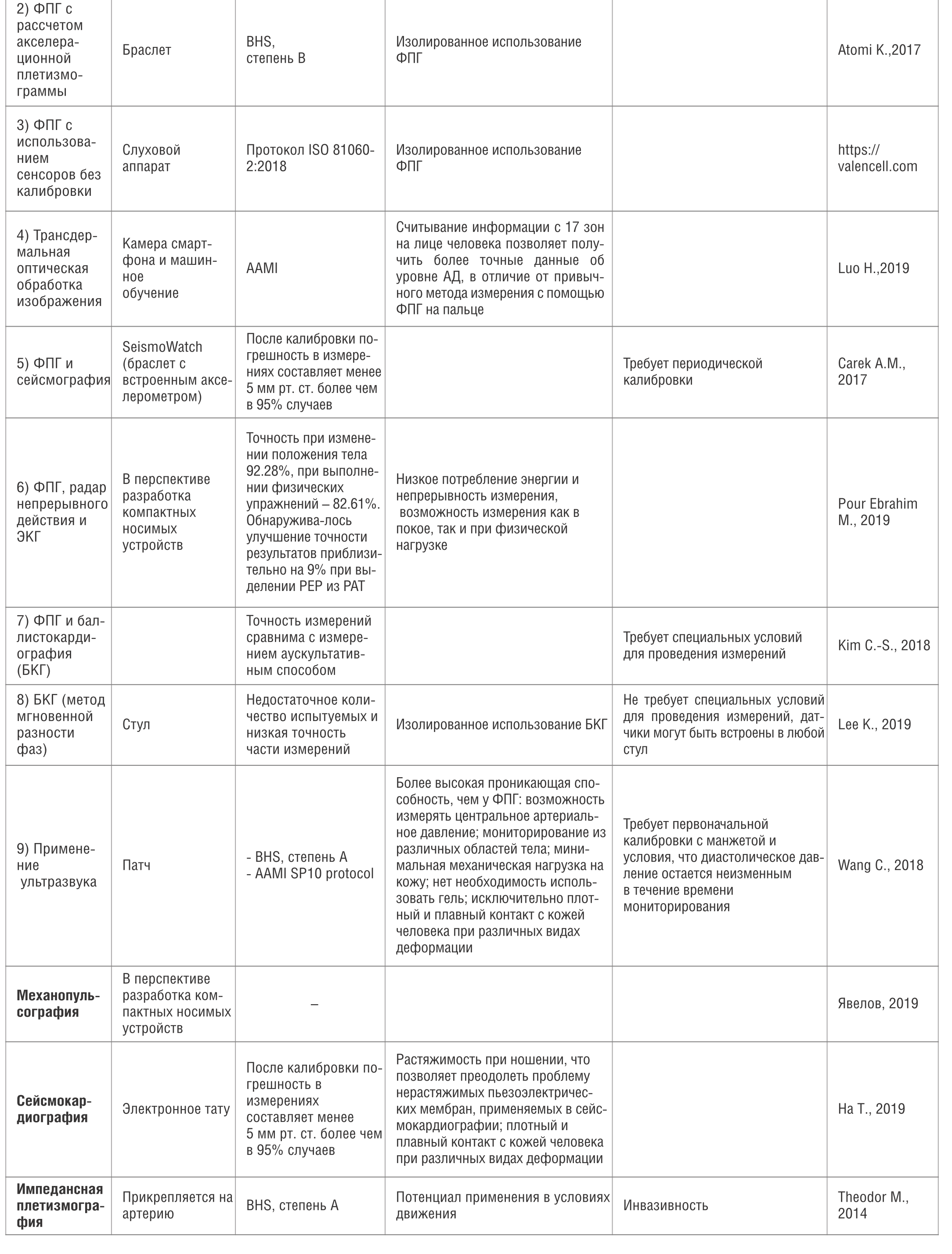
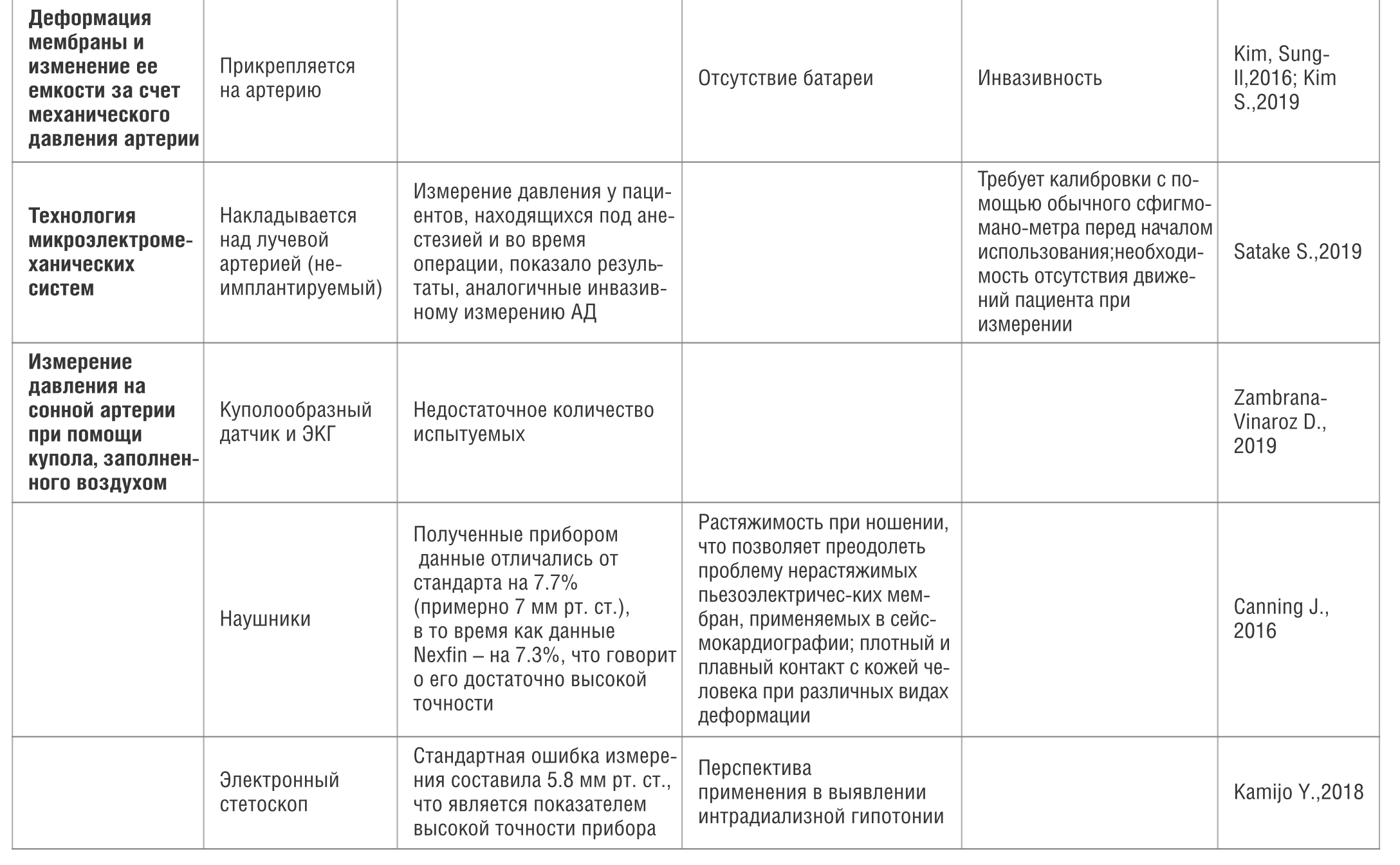
Таблица 1. Технологии и устройства неинвазивного измерения АД
Table 1. Technologies and devices for non-invasive blood pressure measurement
ВЫВОДЫ
- Существующие традиционные методы неинвазивного измерения АД не могут обеспечить его продолжительное мониторирование, так как осуществляют измерение только при неподвижном положении пациента. Тенденции в разработке современных методов направлены на возможность мониторинга при различной физической активности пациента.
- Некоторые технологии показали достаточно точные результаты измерений по сравнению с «золотым стандартом». Однако большинство решений находится на низкой стадии разработки, существуют только в виде единичных прототипов или же не прошли клинические исследования в условиях, необходимых для валидации прибора как медицинского устройства. На данном этапе им предстоит пройти клинические испытания на больших группах пациентов. В связи с этим есть основания ожидать их появления в медицинской практике уже в ближайшее время.
- Большой поток информации, возникающий в процессе функционирования современных приборов, требует разработки инструментов работы с полученными массивами данных.
- Технические инновации в сфере неинвазивного продолжительного мониторирования АД позволят создать новую превентивную модель лечения артериальной гипертензии. Она будет представлять собой закрытую систему, включающую прибор длительного мониторирования и комплекс мер, подобранных в соответствии с результатами мониторинга, что позволит компенсировать патологическую функцию, а также избежать значительных проявлений заболевания за счет поддержания нормального для пациента АД. Вслед за разработкой методов системного мониторинга станет возможным гибкое управление каждой индивидуальной ситуацией также, как и при сахарном диабете.
- Важно понимать, что инновации в сфере мониторинга АД не отменят, а эволюционно дополнят существующие методы регулярного измерения АД. Стандартные технологии и новые решения будут развиваться вместе и дополнять, а не взаимоисключать друг друга, при этом традиционные методы помогут построить новые алгоритмы.
ЛИТЕРАТУРА
- Steinhubl SR, Topol EJ. A skin patch for sensing blood pressures. Nat Biomed Eng 2018; 2: 633–634. doi: 10.1038/s41551-018-0296-9
- Чазова И.Е., Жернакова Ю.В. от имени экспертов. Клинические рекомендации. Диагностика и лечение артериальнои гипертонии. Системные гипертензии 2019;16(1):6–31. doi: 10.26442/2075082X.2019.1.190179. [Chazova I.E., Zhernakova Yu.V.on behalf of experts. Clinical guidelines. Diagnosis and treatment of arterial hypertension]. Sistemnye gipertenzii=Systemic hypertension. 2019;16(1):6–31. doi: 10.26442/2075082X.2019.1.190179. (In Russian)].
- Nimri R, Nir J, Phillip M. Insulin Pump Therapy: Am J Ther 2020; 27: e30–e41. doi: 10.1097/MJT.0000000000001097
- Štechová K. Insulin pump therapy: education and its goals. Vnitr Lek 2019; 65: 248–255.
- Campbell M, Pillarisetty LS. Physiology, Korotkoff Sound. In: StatPearls. Treasure Island (FL): StatPearls Publishing, http://www.ncbi. nlm.nih.gov/books/NBK539778/ (2020, accessed 31 January 2020).
- Wu H, Wang B, Zhu X, Chu G, Zhang Z. A new automatic blood pressure kit auscultates for accurate reading with a smartphone: A diagnostic accuracy study. Medicine (Baltimore) 2016; 95: e4538. doi: 10.1097/MD.0000000000004538
- Peng R-C, Yan W-R, Zhang N-L, Lin W-H, Zhou X-L, Zhang Y-T. Cuffless and Continuous Blood Pressure Estimation from the Heart Sound Signals. Sensors 2015; 15: 23653–23666. doi:10.3390/s150923653
- Oliveira J, Nogueira M, Ramos C, Renna F, Ferreira C, Coimbra M. Using Soft Attention Mechanisms to Classify Heart Sounds. 2019 41st Annual International Conference of the IEEE Engineering in Medicine and Biology Society (EMBC) 2019:6669-6672. doi:10.1109/ embc.2019.8856748.
- Muntner P, Shimbo D, Carey RM, Charleston JB, Gaillard T, Misra S et al. Measurement of Blood Pressure in Humans: A Scientific Statement From the American Heart Association. Hypertension 2019;73. doi: 10.1161/HYP.0000000000000087.
- Kario K, Shimbo D, Tomitani N, Kanegae H, Schwatz JE, Williams B. The first study comparing a wearable watch type blood pressure monitor with a conventional ambulatory blood pressure monitor on in office and out of office settings. J Clin Hypertens 2020; jch.13799. doi: 10.1109/EMBC.2019.8856748
- H2-BP [Электронный ресурс]. URL: https://h2care.com/ (дата обращения: 12.01.2020). [H2-BP [Electronic resource]. URL: https://h2care.com/ (accessed 12.01.2020)].
- Carlson DJ, Dieberg G, Mcfarlane JR, Smart NA. Blood pressure measurements in research: suitability of auscultatory, beat-to-beat, and ambulatory blood pressure measurements. Blood Press Monit 2019; 24: 18–23. doi: 10.1097/MBP.0000000000000355
- Moraes J, Rocha M, Vasconcelos G, Vasconcelos FJ, de Albuquerque V, Alexandria A. Advances in Photopletysmography Signal Analysis for Biomedical Applications. Sensors 2018; 18: 1894. doi: 10.3390/s18061894
- Liu J, Yan BP, Zhang YT, Ding XR, Su P, Zhao N. Multi-Wavelength Photoplethysmography Enabling Continuous Blood Pressure Measurement With Compact Wearable Electronics. IEEE Trans Biomed Eng 2019; 66: 1514–1525. doi: 10.1109/TBME.2018.2874957
- Elgendi M, Fletcher R, Liang Y, Howard N, Lovell N, Abbott D, et al. The use of photoplethysmography for assessing hypertension. Npj Digit Med 2019; 2: 60. doi: 10.1038/s41746-019-0136-7
- Wang C, Li X, Hu H, Zhang L, Huang Z, Lin M, et al. Monitoring of the central blood pressure waveform via a conformal ultrasonic device. Nat Biomed Eng 2018; 2: 687–695. doi: 10.1038/s41551-018-0287-x
- Atomi K, Kawanaka H, Bhuiyan MdS, Oguri K. Cuffless Blood Pressure Estimation Based on Data-Oriented Continuous Health Monitoring System. Comput Math Methods Med 2017; 2017: 1–10. doi: 10.1155/2017/1803485
- Cuff-less, All-PPG Blood Pressure Monitoring Technology from Valencell [Электронный ресурс]. URL: https://valencell.com/bloodpressure/ (дата обращения: 14.01.2020).
- Luo H, Yang D, Barszczyk A, Vempala N, Wei J, Wu SJ, et al. Smartphone-Based Blood Pressure Measurement Using Transdermal Optical Imaging Technology. Circ Cardiovasc Imaging; 12. Epub ahead of print August 2019. doi: 10.1161/CIRCIMAGING.119.008857.
- Carek AM, Conant J, Joshi A, Kang H, Inan OT. SeismoWatch: Wearable Cuffless Blood Pressure Monitoring Using Pulse Transit Time. Proc ACM Interact Mob Wearable Ubiquitous Technol 2017; 1: 1–16. doi: 10.1145/3130905
- Inan OT, Migeotte P-F, Park K-S, Etemadi M, Tavakolian K, Casanella R, et al. Ballistocardiography and Seismocardiography: A Review of Recent Advances. IEEE J Biomed Health Inform 2015; 19: 1414– 1427. doi: 10.1109/JBHI.2014.2361732
- Pour Ebrahim M, Heydari F, Wu T, Walker K, Joe K, Redoute J-M, et al. Blood Pressure Estimation Using On-body Continuous Wave Radar and Photoplethysmogram in Various Posture and Exercise Conditions. Sci Rep 2019; 9: 16346. doi: 10.1038/s41598-019-52710-8
- Deuchar DC. Ballistocardiography Heart 1967;29(3):285–288. doi: 10.1136/hrt.29.3.285.
- Kim C-S, Carek AM, Inan OT, Mukkamala R, Hahn J-O. Ballistocardiogram-Based Approach to Cuffless Blood Pressure Monitoring: Proof of Concept and Potential Challenges. IEEE Trans Biomed Eng 2018; 65: 2384–2391. doi: 10.1109/TBME.2018.2797239
- Lee K, Roh J, Cho D, Hyeong J, Kim S. A Chair-Based Unconstrained/Nonintrusive Cuffless Blood Pressure Monitoring System Using a Two-Channel Ballistocardiogram. Sensors 2019; 19: 595. doi: 10.3390/s19030595
- Beulen BWAMM, Bijnens N, Koutsouridis GG, et al. Toward Noninvasive Blood Pressure Assessment in Arteries by Using Ultrasound. Ultrasound Med Biol 2011; 37: 788–797.
- Kim I, Bhagat YA. Towards development of a mobile RF Doppler sensor for continuous heart rate variability and blood pressure monitoring. In: 2016 38th Annual International Conference of the IEEE Engineering in Medicine and Biology Society (EMBC). Orlando, FL, USA: IEEE, pp. 3390–3393. doi: 10.1109/EMBC.2016.7591455
- Явелов И.С. Механопульсография и основные феномены сердечно-сосудистой системы. М.: Институт компьютерных исследований, 2019. 194 с. [Yаvelov I.S. Mechanopulsography and the main phenomena of the cardiovascular system. M.: Institute for Computer Research, 2019.194 s., 2019. 194 p. (In Russian)].
- Ha T, Tran J, Liu S, Jang H, Jeong H, Mitbander R, et al. A Chest Laminated Ultrathin and Stretchable E Tattoo for the Measurement of Electrocardiogram, Seismocardiogram, and Cardiac Time Intervals. Adv Sci 2019; 1900290. doi: 10.1002/advs.201900290
- Nguyen H, Kieu H, Wang Z, Lee H N.D. Three-dimensional facial digitization using advanced digital image correlation. Appl Opt 2018; 57: 2188. doi: 10.1364/AO.57.002188
- Potkay JA. Long term, implantable blood pressure monitoring systems. Biomed Microdevices 2008; 10: 379–392. doi: 10.1007 /s10544-007-9146-3
- Ruh D, Sherman S, Theodor M, Ruhhammer J, Foerster K, Heilmann C, et al. Determination of vessel wall dynamics by optical microsensors. In: 2012 Annual International Conference of the IEEE Engineering in Medicine and Biology Society. San Diego, CA: IEEE, pp. 2359–2362. doi: 10.1109/EMBC.2012.6346437
- Ruhhammer J, Ruh D, Foerster K, Heilmann C, Beyersdoff F, Barker A, et al. Arterial strain measurement by implantable capacitive sensor without vessel constriction. In: 2012 Annual International Conference of the IEEE Engineering in Medicine and Biology Society. San Diego, CA: IEEE, pp. 535–538. doi: 10.1109/EMBC.2012.6345986
- Theodor M, Fiala J, Ruh D, Foerster K, Heilmann C, Beyersdoff F, et al. Implantable accelerometer system for the determination of blood pressure using reflected wave transit time. Sens Actuators Phys 2014; 206: 151–158. doi: 10.1016/j.sna.2013.12.006
- Theodor M, Ruh D, Ocker M, Spether D, Foerster K, Heilmann C, et al. Implantable impedance plethysmography. Sens Switz 2014; 14: 14858–14872. doi: 10.3390/s140814858
- Kim S, Park J, So S, Ahn S, Choi J, Koo C, et al. Characteristics of an Implantable Blood Pressure Sensor Packaged by Ultrafast Laser Microwelding. Sensors 2019; 19: 1801. doi: 10.3390/s19081801
- Kim, Sung-Il, Kim, Eung-Bo, So S-k, 최지연, Joung Y-H. Quatrz 웨이퍼의 직접접합과 극초단 레이저 가공을 이용한 체내 이식 형 혈압센서 개발. 대한의용생체공학회:의공학회지 2016; 37: 168–177. doi: https://doi.org/10.9718/JBER.2016.37.5.168
- Satake S, Shimura T, Ono T, Shimomura K, Takenoshita S, Kono K. Noninvasive continuous blood pressure monitoring using microelectromechanical system technology: Blood Press Monit 2019; 24: 155–159. doi: 10.1097/MBP.0000000000000380
- Zambrana-Vinaroz D, Vicente-Samper J, G. Juan C, Esteve-Sala V, Sabater-Navarro J. Non-Invasive Device for Blood Pressure Wave Acquisition by Means of Mechanical Transducer. Sensors 2019; 19: 4311. doi: 10.3390/s19194311
- Canning J, Helbert K, Iashin G, Matthews J, Yang J, Delano MK, et al. Noninvasive and continuous blood pressure measurement via superficial temporal artery tonometry. In: 2016 38th Annual International Conference of the IEEE Engineering in Medicine and Biology Society (EMBC). Orlando, FL, USA: IEEE, pp. 3382–3385. doi: 10.1109/ EMBC.2016.7591453
- Kamijo Y, Kanda E, Horiuchi H, Kounoue N, Ono K, Maeda K, et al. Continuous monitoring of blood pressure by analyzing the blood flow sound of arteriovenous fistula in hemodialysis patients. Clin Exp Nephrol 2018; 22: 677–683. doi: 10.1007/s10157-017-1499-1
- Reeves PB, Mc Causland FR. Mechanisms, Clinical Implications, and Treatment of Intradialytic Hypotension. Clin J Am Soc Nephrol 2018; 13: 1297–1303. doi: 10.2215/CJN.12141017
- Kobalava ZD, Kotovskaya YV, Babaeva LA, Moiseev VS. Validation of TM-2655 oscillometric device for blood pressure measurement: Blood Press Monit 2006; 11: 87–90. doi:10.1097/01.mbp.0000200484.49540.12
- Иванов С. Ю., Бондаренко Б. Б. Неинвазивные методы исследования динамики артериального давления. Артериальная гипертензия 2018;24(6):637–645. doi:10.18705/1607-419X-2018-24-6-637-645 [Ivanov S. YU., Bondarenko B. B. Non-invasive methods for studying the dynamics of blood pressure. Arterial'naya gipertenziya=Arterial hypertension. 2018;24(6):637–645. doi:10.18705/1607-419X-2018-24-6-637-645. (In Russian)].